题目内容
根据水溶液中存在的平衡关系,判断下列说法正确的是( )
| A、往水中滴加少量稀硫酸,能促进水电离 |
| B、室温下,稀释0.1mol?L-1的醋酸,溶液中所有离子的浓度均降低 |
| C、往AgCl悬浊液中加入0.1mol?L-1Na2S溶液,有黑色沉淀产生 |
| D、浓度均为0.1 mol?L-1的溶液,pH由大到小排列顺序为:NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:A、稀硫酸抑制水的电离;
B、平衡状态下离子浓度减小,离子积常数分析氢氧根离子浓度增大;
C、硫化银溶解度小于氯化银;
D、硫酸氢钠溶液中完全电离显酸性,硫酸铵溶液铵根离子水解显酸性.
B、平衡状态下离子浓度减小,离子积常数分析氢氧根离子浓度增大;
C、硫化银溶解度小于氯化银;
D、硫酸氢钠溶液中完全电离显酸性,硫酸铵溶液铵根离子水解显酸性.
解答:
解:A、稀硫酸抑制水的电离,往水中滴加少量稀硫酸,能抑制水电离,故A错误;
B、温下,稀释0.1mol?L-1的醋酸,平衡状态下离子浓度减小,氢离子浓度减小,依据离子积常数可知氢氧根离子浓度增大,故B错误;
C、硫化银溶解度小于氯化银,往AgCl悬浊液中加入0.1mol?L-1Na2S溶液,实现程度转化,有黑色沉淀产生,故C正确;
D、硫酸氢钠溶液中完全电离显酸性,硫酸铵溶液铵根离子水解显酸性,浓度均为0.1 mol?L-1的溶液,pH由大到小排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4,故D错误;
故选C.
B、温下,稀释0.1mol?L-1的醋酸,平衡状态下离子浓度减小,氢离子浓度减小,依据离子积常数可知氢氧根离子浓度增大,故B错误;
C、硫化银溶解度小于氯化银,往AgCl悬浊液中加入0.1mol?L-1Na2S溶液,实现程度转化,有黑色沉淀产生,故C正确;
D、硫酸氢钠溶液中完全电离显酸性,硫酸铵溶液铵根离子水解显酸性,浓度均为0.1 mol?L-1的溶液,pH由大到小排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4,故D错误;
故选C.
点评:本题考查了水的电离平衡影响因素,沉淀转化,盐类水解溶液酸碱性分析判断,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列区分植物油和矿物油的方法中,正确的是( )
| A、点燃,能燃烧的为矿物油 |
| B、加入水中,浮在水面上的为植物油 |
| C、加入足量的NaOH溶液共煮,不再分层的为植物油 |
| D、尝一尝,能食用的为植物油 |
下列有关推断正确的是( )
| A、SO3 是酸性氧化物,能与NaOH溶液反应 |
| B、Na2O、Na2O2组成元素相同,与CO2反应产物也相同 |
| C、酸酐一定是氧化物,金属氧化物一定是碱性氧化物 |
| D、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
下列气体不会造成空气污染的是( )
| A、NO |
| B、NO2 |
| C、N2 |
| D、SO2 |
下列关于pH=3的盐酸和醋酸溶液的说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量分别为a和b,则a<b |
| C、加入足量的铁粉,放出H2的体积相同 |
| D、分别用蒸馏水稀释m倍和n倍,两溶液pH仍相同,则m=n |
在2FeCl2+Cl2=2FeCl3的反应中,还原剂是( )
| A、Cl2 |
| B、FeCl2 |
| C、Fe |
| D、FeCl3 |
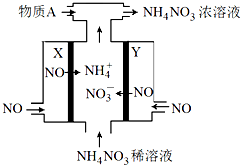 电解NO制备 NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是
电解NO制备 NH4NO3的工作原理如图所示,X、Y皆Pt电极,为使电解产物全部转化为NH4NO3,需补充物质A.下列说法正确的是( )
| A、物质A为NH3 |
| B、X电极为电解池阳极 |
| C、Y电极上发生了还原反应 |
| D、Y电极反应式为NO-3e-+4OH-═NO3-+2H2O |
由于环境原因,最近常出现雾霾天气,严重影响人体健康,还容易造成事故. 雾属于下列哪种分散系( )
| A、乳浊液 | B、溶液 |
| C、胶体 | D、悬浊液 |