题目内容
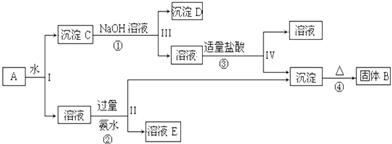
3.某学校化学兴趣小组为探索金属回收物的综合利用,专门设计实验用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4•7H2O)和胆矾晶体(CuSO4•5H2O),其实验方案如下:
请回答下列问题:
(1)过滤用的玻璃仪器有烧杯、漏斗、玻璃棒.
(2)在滤液C转化为沉淀Ⅱ的过程中盐酸的用量不易控制,可改为通CO2气体,写出滤液C中通入过量CO2的离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.写出由沉淀Ⅱ转化为AlCl3溶液的离子方程式:Al(OH)3+3H+═Al3++3H2O.
(3)小组成员经过检测,发现制得的绿矾不纯,试分析其主要含有哪些杂质:氯化钠、硫酸钠、硫酸铁,要想由沉淀Ⅰ最终制得纯度较高的绿矾,应如何改进向溶液D中加入足量铁粉,反应后过滤,再将滤液蒸发浓缩、冷却结晶、过滤即可得纯度较高的绿矾
(4)小组成员从资料中获知H2O2是一种绿色氧化剂,在滤渣B中加入稀硫酸和H2O2来制备胆矾晶体,则该反应的总化学方程式为Cu+H2O2+H2SO4+3H2O═CuSO4•5H2O(或Cu+H2O2+H2SO4═CuSO4+2H2O.
(5)有同学提出可将方案中最初溶解合金的盐酸改为烧碱,重新设计方案,也能最终制得三种物质,你认为第二种方案相对于第一种方案更合理(填“更合理”或“不合理”),理由是一种方案操作步骤多、时间长、消耗试剂量大.
分析 合金铝、铁、铜加入足量盐酸溶解后过滤,得到滤液A为氯化铝、氯化亚铁,加入足量氢氧化钠溶液过滤得到滤液C为偏铝酸钠溶液,加入适量盐酸过滤得到氢氧化铝沉淀,氢氧化铝加入盐酸溶解生成氯化铝溶液;沉淀Ⅰ为氢氧化亚铁,加入硫酸生成硫酸亚铁,溶液D蒸发结晶得到绿矾晶体,
(1)根据过滤实验用到的仪器来回答;
(2)滤液C中含有偏铝酸钠,通入过量CO2生成氢氧化铝沉淀和碳酸氢钠,沉淀Ⅱ为氢氧化铝,与盐酸反应转化为AlCl3溶液;
(3)制得的绿矾不纯,部分亚铁离子被氧化为铁离子,要想由沉淀I最终制得纯度较高的绿矾,需要向D溶液中加入过量铁粉还原铁离子过滤后溶液通过操作得到晶体;
(4)铜、稀硫酸、双氧水的性质来判断反应的发生,并结合质量守恒定律写出该反应的化学方程式;
(5)根据实验中的酸和碱的量的情况来对比回答.
解答 解:合金铝、铁、铜加入足量盐酸溶解后过滤,得到滤液A为氯化铝、氯化亚铁,加入足量氢氧化钠溶液过滤得到滤液C为偏铝酸钠溶液,加入适量盐酸过滤得到氢氧化铝沉淀加入盐酸溶解生成氯化铝溶液;沉淀Ⅰ为氢氧化亚铁,加入硫酸生成硫酸亚铁溶液D蒸发结晶得到绿矾晶体,
(1)过滤实验用到的仪器有:滤纸、铁架台、铁圈、烧杯、玻璃棒和漏斗,故答案为:烧杯、漏斗、玻璃棒;
(2)滤液C中含有偏铝酸钠,通入过量CO2生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,沉淀Ⅱ为氢氧化铝,与盐酸反应转化为AlCl3溶液,反应的离子方程式为Al(OH)3+3H+═Al3++3H2O,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;Al(OH)3+3H+═Al3++3H2O;
(3)发现制得的绿矾不纯,含有氯化钠、硫酸钠、硫酸铁,是因为亚铁离子被氧化为铁离子,要想由沉淀I最终制得纯度较高的绿矾,需要向D溶液中加入过量铁粉还原铁离子为亚铁离子,过滤得到溶液蒸发浓缩,冷却结晶,过滤洗涤得到绿矾晶体;
故答案为:氯化钠、硫酸钠、硫酸铁;向溶液D中加入足量铁粉,反应后过滤,再将滤液蒸发浓缩、冷却结晶、过滤即可得纯度较高的绿矾;
(4)铜与浓硫酸反应生成有毒有污染的二氧化硫气体,若铜先和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所以途径②最佳,Cu中加入稀硫酸和H2O2可以制备胆矾晶体,反应方程式为:Cu+H2O2+H2SO4+3H2O═CuSO4•5H2O(或Cu+H2O2+H2SO4═CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4+3H2O═CuSO4•5H2O(或Cu+H2O2+H2SO4═CuSO4+2H2O);
(5)在实验原方案中,需要的是适量的酸,且步骤繁琐,这很难控制,改用烧碱,首先分离出来铝,然后加入硫酸,分离出铁,最后得铜的化合物,故比较合理,
故答案为:更合理;前一种方案操作步骤多、时间长、消耗试剂量大.
点评 本题考查物质的制备,为高考常见题型,题目涉及常见仪器的使用方法、物质的分离和提纯等知识,难度中等,试题涉及的题量稍大,知识点较多,充分考查了学生分析、理解能力及灵活应用所学知识的能力.

| A. | Na+ | B. |  | C. |  | D. |  |
| 周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | e | f | h | |||||
| 3 | a | c | d | g | i | j | r | |
| 4 | b |
(2)a元素位于第三周期第IA族,它的元素符号是Na;
(3)e元素原子的最外层电子数为4;
(4)a、b、c三种元素的最高价氧化物对应水化物中碱性最弱的是Mg(OH)2(填化学式);
(5)h元素和i元素均可形成气态氢化物,其稳定性为H2h>H2i(填“大于”或“小于”);
(6)c元素和j元素形成化合物的化学式是MgCl2;
(7)j元素的单质跟氢气点燃的化学反应方程式:Cl2+H2$\frac{\underline{\;点燃\;}}{\;}$2HCl;
(8)b元素的单质与水反应的离子方程式:2K+2H2O=2OH-+2K++H2↑;
(9)f元素和g元素两者核电荷数之差是8.
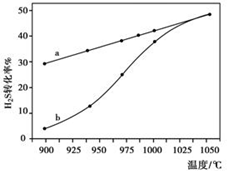
(1)方法一:H2S热分解法,反应式为:2H2S(g)?2H2(g)+S2(g)△H 在恒容密闭容器中,控制不同温度进行H2S的分解实验.H2S的起始浓度均为c mol•L-1.不同温度下反应相同时间t后,测得如图所示H2S转化率曲线图.其中a为平衡转化率与温度关系曲线,b为未达到平衡时转化率与温度的关系曲线.
①△H>0(“>”、“<”或“=”),
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则tmi
 n内反应速率v(H2)=$\frac{0.4c}{t}$mol/(L•min)(用含c、t的代数式表示).
n内反应速率v(H2)=$\frac{0.4c}{t}$mol/(L•min)(用含c、t的代数式表示).③请说明随温度的升高,曲线b向曲线a逼近的原因:温度的升高,反应速率加快,达到平衡所需时间缩短.
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.反应装置由气化炉和燃烧炉两个反应器组成,相关反应如下表所示:
| 流程1:气化炉中产生H2 | 流程2:燃烧炉中CaO再生 |
| 通入水蒸气,主要化学反应: I:C(s)+H2O(g)?CO(g)+H2(g) K1 II:CO(g)+H2O(g)?CO2(g)+H2(g) K2 III:CaO(s)+CO2(g)?CaCO3(s) K3 | 通入纯氧,主要化学反应: IV:C(s)+O2(g)=CO2(g)△H=-393.8kJ•mol-1 V:CaCO3(s)=CaO(s)+CO2(g) |
②对于可逆反应C(s)+2H2O(g)+CaO(s)?CaCO3(s)+2H2(g),△H=-87.9kJ•mol-1;采取以下措施可以提高H2产量的是AC.(填字母编号)
A.降低体系的温度 B.使各气体组分浓度均加倍
C.适当增加水蒸气的通入量 D.增加CaO的量,提高CO2的吸收率
(3)方法二与方法一相比其优点有实现了吸收剂CaO的循环,降低能耗(写一个即可).
| A. | FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+ | |
| B. | 将NH3通入H2SO4溶液中:NH3+H+=NH4+ | |
| C. | FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- | |
| D. | H2SO4溶液与Ba(OH)2溶液混合:H++OH-=H2O |
| A. | CO2的比例模型: | |
| B. | 氢氧根离子的电子式: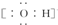 | |
| C. | 氯原子的结构示意图: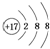 | |
| D. | 中子数为146、质子数为92的铀(U)原子:${\;}_{92}^{146}$U |