题目内容
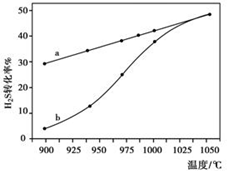
15.氢气是清洁的能源,也是重要的化工原料,有关氢气的制取研究是一个有趣的课题.根据提供两种制氢方法,完成下列各题:(1)方法一:H2S热分解法,反应式为:2H2S(g)?2H2(g)+S2(g)△H 在恒容密闭容器中,控制不同温度进行H2S的分解实验.H2S的起始浓度均为c mol•L-1.不同温度下反应相同时间t后,测得如图所示H2S转化率曲线图.其中a为平衡转化率与温度关系曲线,b为未达到平衡时转化率与温度的关系曲线.
①△H>0(“>”、“<”或“=”),
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,则tmi
 n内反应速率v(H2)=$\frac{0.4c}{t}$mol/(L•min)(用含c、t的代数式表示).
n内反应速率v(H2)=$\frac{0.4c}{t}$mol/(L•min)(用含c、t的代数式表示).③请说明随温度的升高,曲线b向曲线a逼近的原因:温度的升高,反应速率加快,达到平衡所需时间缩短.
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2.反应装置由气化炉和燃烧炉两个反应器组成,相关反应如下表所示:
| 流程1:气化炉中产生H2 | 流程2:燃烧炉中CaO再生 |
| 通入水蒸气,主要化学反应: I:C(s)+H2O(g)?CO(g)+H2(g) K1 II:CO(g)+H2O(g)?CO2(g)+H2(g) K2 III:CaO(s)+CO2(g)?CaCO3(s) K3 | 通入纯氧,主要化学反应: IV:C(s)+O2(g)=CO2(g)△H=-393.8kJ•mol-1 V:CaCO3(s)=CaO(s)+CO2(g) |
②对于可逆反应C(s)+2H2O(g)+CaO(s)?CaCO3(s)+2H2(g),△H=-87.9kJ•mol-1;采取以下措施可以提高H2产量的是AC.(填字母编号)
A.降低体系的温度 B.使各气体组分浓度均加倍
C.适当增加水蒸气的通入量 D.增加CaO的量,提高CO2的吸收率
(3)方法二与方法一相比其优点有实现了吸收剂CaO的循环,降低能耗(写一个即可).
分析 (1)①升高温度,化学平衡向着吸热方向进行,据此判断;
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,
2H2S(g)→2H2(g)+S2(g)
开始:c 0 0
转化:0.4c 0.4c 0.2c
平衡:0.6c 0.4c 0.2c
根据v=$\frac{△c}{△t}$进行计算;
③温度的升高,反应速率加快,使曲线b向曲线a逼近;
(2)①反应I、II、III之和为反应C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g),据此分析;
②提高H2产量,则需使平衡正向移动,根据影响平衡的因素分析;
(3)方法二CaO能循环使用,据此分析.
解答 解:(1)①根据图示内容知道,随着温度的升高,硫化氢的转化率逐渐增大,所以化学平衡正向移动,即化学反应是吸热的,则△H>0,故答案为:>;
②若985℃时,反应经t min达到平衡,此时H2S的转化率为40%,
2H2S(g)→2H2(g)+S2(g)
开始:c 0 0
转化:0.4c 0.4c 0.2c
平衡:0.6c 0.4c 0.2c
根据v=$\frac{△c}{△t}$=$\frac{0.4c}{t}$mol/(L•min),故答案为:$\frac{0.4c}{t}$mol/(L•min);
③温度的升高,反应速率加快,使曲线b向曲线a逼近,故答案为:温度的升高,反应速率加快,达到平衡所需时间缩短;
(2)①已知:I:C(s)+H2O(g)═CO(g)+H2(g) K1
Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g)K2
Ⅲ:CaO(s)+CO2(g)═CaCO3(s)K3
反应I、II、III之和为反应C(s)+2H2O(g)+CaO(s)═CaCO3(s)+2H2(g),则K=K1•K2•K3;
故答案为:K1•K2•K3;
②提高H2产量,则需使平衡正向移动,已知C(s)+2H2O(g)+CaO(s)?CaCO3(s)+2H2(g),△H=-87.9kJ•mol-1;
A.该反应为放热反应,降低体系的温度,平衡正移,则能提高H2产量,故A正确;
B.该反应前后气体体积不变,使各气体组分浓度均加倍,则压强增大,平衡不移动,所以H2产量不变,故B错误;
C.适当增加水蒸气的通入量,平衡正移,则能提高H2产量,故C正确;
D.增加CaO的量,对平衡无影响,所以H2产量不变,故D错误;
故答案为:AC;
(3)方法二中实现了吸收剂CaO的循环,降低能耗,降低了生产成本,故答案为:实现了吸收剂CaO的循环,降低能耗.
点评 本题考查反应热的判断、反应速率的计算、化学平衡图象与影响因素等,难度中等,注意把握图象中坐标的含义,充分利用图象中的信息,题目综合性强,侧重于考查学生对所学知识的应用能力.

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案(1)Fe单质为体心立方晶体,晶胞中铁原子的配位数为8,基态铁原子有4个未成对电子,Fe3+的电子排布式为1s22s22p63s23p63d6;.
(2)硝酸钾中NO3-的空间构型为平面正三角形,写出与NO3-互为等电子体的一种非极性分子化学式BF3[SO3(g)、BBr3等].
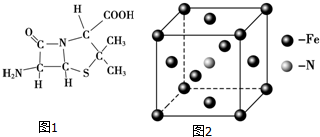
(3)6氨基青霉烷酸的结构如图1所示,其中采用sp3杂化的原子有C、N、O、S.
(4)下列说法正确的有a(填字母序号).
a.乙醇分子间可形成氢键,导致其沸点比氯乙烷高
b.钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显-1价
c.聚乙烯(
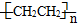 )分子中有5n个σ键
)分子中有5n个σ键d.由下表中数据可确定在反应Si(s)+O2(g)═SiO2(s)中,每生成60g SiO2放出的能量为(2c-a-b) kJ
| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
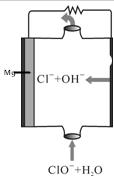
| A. | 电子由负极经电解质溶液移向正极 | |
| B. | ClO-参与的一极为正极 | |
| C. | 电池中镁为负极,发生氧化反应 | |
| D. | 放电过程中,溶液中Cl-的物质的量不变 |
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
(1)以上步骤有错误的是(填编号)①,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)偏大.
(2)判断滴定终点的现象是:无色变为粉红色,半分钟内不变色.
(3)根据下列数据:请计算待测盐酸溶液的浓度:0.20mol/L.
滴定次数 | 待测体积(mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.40 | 20.40 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00- | 24.00 |
| A. | 碳酸盐 | B. | 钾盐 | C. | 酸式盐 | D. | 正盐 |
