题目内容
5.短周期主族元素A、B、C、D的原子序数依次增大,A、B、C原子的最外层电子数之和为12,B、C、D位于同一周期,C原子的最外层电子数既是A原子内层电子数的3倍又是B原子最外层电子数的3倍.下列说法正确的是( )| A. | 原子半径:B>A,离子半径C<D | |
| B. | B的单质能与A的最高价氧化物发生置换反应 | |
| C. | 元素B和D能形成BD2型的共价化合物 | |
| D. | D的单质有毒,且干燥的单质D有漂白性 |
分析 C原子的最外层电子数是B原子最外层电子数的3倍,则二者的最外层电子数应为偶数,A、B、C原子的最外层电子数之和为12,则A的最外层电子数为偶数,C原子的最外层电子数既是A原子内层电子数的3倍,则C的最外层电子数为6,B的最外层电子数为2,A的最外层电子数为4,则A为C元素,B、C、D位于同一周期,应为第三周期元素,C为S元素,B为Mg元素,则D应为Cl元素,结合元素对应单质、化合物的性质解答该题.
解答 解:C原子的最外层电子数是B原子最外层电子数的3倍,则二者的最外层电子数应为偶数,A、B、C原子的最外层电子数之和为12,则A的最外层电子数为偶数,C原子的最外层电子数既是A原子内层电子数的3倍,则C的最外层电子数为6,B的最外层电子数为2,A的最外层电子数为4,则A为C元素,B、C、D位于同一周期,应为第三周期元素,C为S元素,B为Mg元素,则D应为Cl元素,
根据分析可知:A为C,B为Mg,C为S,D为Cl,
A.A为C、B为Mg,原子半径Mg>C;C为S、D为Cl,硫离子与氯离子的电子层数相同,电荷守恒越大,离子半径越小,则离子半径:C>D,故A错误;
B.Mg与二氧化碳反应的方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,该反应为置换反应,故B正确;
C.B为Mg,D为Cl,二者形成的化合物为离子化合物,故C错误;
D.D为Cl,其单质为氯气,干燥的氯气没有漂白性,故D错误;
故选B.
点评 本题考查原子结构与元素周期律的应用,题目难度中等,推断元素为解答关键,注意根据核外电子关系特点判断元素的种类,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
15.现有Fe、FeO、Fe2O3和Fe3O4组成的混合物,取一定质量,加入100mL2mol/L的盐酸,混合物恰好完全溶解,放出a mL(标准状况下)的气体,所得溶液中加入KSCN溶液无血红色出现.若取等质量的该混合物,用足量的CO还原可得铁单质的质量为( )
| A. | 11.2 g | B. | 5.6g | C. | 8.4g | D. | 2.8g |
16.在一定条件下的恒温恒容容器中,当下列物理量不再发生变化时,反应:2A(g)+B(g)?3C(g)+D(s)不能表明已达平衡状态的是( )
| A. | B的体积分数 | B. | 气体平均相对分子质量 | ||
| C. | 气体的总压强 | D. | 混合气体的密度 |
13.下列叙述不正确的是( )
| A. | 同一周期原子半径从左到右依次减小 | |
| B. | 同一主族元素的化学性质相同 | |
| C. | 同一周期元素最高化合价从左到右不一定增大 | |
| D. | 同一主族元素的化学性质相似 |
20.现有一Na2SO3、Na2SO4混合物样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是( )
| A. | 将样品配制成溶液V1L,取其中25.00mL恰好与V2mL浓度为cmol/L酸性KMnO4溶液完全反应 | |
| B. | 向样品中加足量H2O2,再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg | |
| C. | 将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为c g | |
| D. | 将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重d g |
10.下列反应中属于加成反应的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | B. | 乙烯使溴水褪色 | ||
| C. | 苯在铁粉存在下与液溴的反应 | D. | 苯的硝化反应 |
17.碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图.下列有关该物质的说法正确的是( )
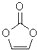

| A. | 1mol该物质最多可与2molH2加成 | B. | 分子式为C3H2O3 | ||
| C. | 分子中只有极性键 | D. | 8.6g该物质完全燃烧得到6.72LCO2 |
15.将c(H+)为10-2mol/L的醋酸和盐酸溶液分别加水稀释100倍,得两溶液的c(H+)分别为a和b,则a和b的关系是( )
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
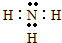
 ,其中含有的化学键有共价键、离子键,属于离子 晶体
,其中含有的化学键有共价键、离子键,属于离子 晶体