题目内容
3.下列说法正确的是( )| A. | 常温下,苯酚易溶于水 | |
| B. | 苯酚俗称石炭酸,具有微弱的酸性,能与碳酸钠溶液反应 | |
| C. | 能与FeCl3溶液作用显紫色的有机物一般含有酚羟基 | |
| D. | 洒落皮肤上的苯酚可以用氢氧化钠稀溶液洗涤 |
分析 A.常温下苯酚在水中溶解度不大;
B.苯酚酸性很弱,与碳酸钠反应生成苯酚钠、碳酸氢钠;
C.酚-OH与氯化铁发生显色反应;
D.NaOH具有强腐蚀性.
解答 解:A.常温下苯酚在水中溶解度不大,因苯环为憎水基团,故A错误;
B.苯酚俗称石炭酸,具有微弱的酸性,与碳酸钠反应生成苯酚钠、碳酸氢钠,故B正确;
C.酚-OH与氯化铁发生显色反应,则能与FeCl3溶液作用显紫色的有机物一般含有酚羟基,故C正确;
D.NaOH具有强腐蚀性,则洒落皮肤上的苯酚可以用酒精洗涤,故D错误;
故选BC.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意性质与用途的关系,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
13.用括号中的试剂除去各组物质中的杂质,可选试剂不正确的是( )
| A. | 乙醇中的水(新制CaO) | B. | 乙烷中乙烯(溴水) | ||
| C. | 苯中的甲苯(溴水) | D. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) |
14.X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
| A. | X的原子半径一定大于Y的原子半径 | |
| B. | Y的离子半径一定大于X的离子半径 | |
| C. | X与Y的简单离子不可能具有相同的电子层结构 | |
| D. | 两元素形成的化合物中,原子个数比不可能为1:1 |
11.下列有机物中不能发生银镜反应的是( )
| A. | 甲酸 | B. | 乙酸 | C. | 甲酸甲酯 | D. | 乙醛 |
18.下列叙述中,正确的是( )
| A. | 某物质中只含有一种元素,该物质一定是纯净物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 离子化合物只含离子键 |
8.下列各装置图的叙述中,错误的是( )
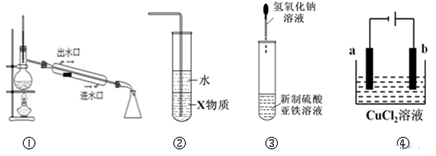

| A. | 实验室用装置①蒸馏石油 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③可用于制备氢氧化亚铁并观察其颜色 | |
| D. | 装置④是电解精炼铜,b极为粗铜,发生氧化反应 |
2.溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-.某同学设计并完成了如图的实验:下列说法正确的是( )


| A. | 溶液 A 中一定存在 NH4+、SO42-、SO32-,可能存在 Na+ | |
| B. | 溶液 A 中一定存在 NH4+、Mg2+、SO42-、SO32-,可能存在 Cl- | |
| C. | 溶液 A 中可能存在 Cl-,且 c(Na+)≥0.20 mol•L-1 | |
| D. | 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+ |
3.设NA为阿伏加德罗常数的值,下列说法中不正确的是( )
| A. | 1molC2H4Cl2中含有共用电子对数目为7NA | |
| B. | 标准状况下,44.8 L丙三醇与足量金属钠反应,生成气体的分子数为3NA | |
| C. | 20℃时,1 mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| D. | 15g甲基正离子(CH3+)所含有的电子数是8NA |
 实验室用氯化钠固体配制1.00mol/L的NaCl溶液500mL,回答下列问题:
实验室用氯化钠固体配制1.00mol/L的NaCl溶液500mL,回答下列问题: