题目内容
3.不能正确表示原子轨道的是( )| A. | 2s | B. | 5f | C. | 2d | D. | 3px |
分析 根据第一层(K层)上只有1S亚层,第二电子层(L层)只有2s和2p亚层,第三电子层(M层)只有3s、3p和3d亚层,第四电子层(N层)只有4s、4p、4d和4f亚层,结合各能级含有的轨道分析,s能级只有1个轨道,p能级有3个轨道,d能级有5个轨道,f能级有7个轨道,注意不存在1p、2d、3f能级,结合选项符号能否指明确定的轨道进行判断.
解答 解:A.2s能级只有1个轨道,故2s可以表示原子轨道,故A不选;
B.第五能层含有5s、5p、5d、5f能级,所以存在5f能级,故B不选;
C.第二能层含有2s、2p两个能级,所以不存在2d能级,故C选;
D.第三能层含有3s、3p、3d三个能级,所以存在3p能级,3p能级含有3个轨道,3个轨道相互垂直,3px表示为x轴上的轨道,故D不选;
故选C.
点评 本题考查了能层中的能级排布,题目难度不大,从能层数与能级数之间的关系分析解答,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14. 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中T单质和H2在光照的条件下发生爆炸.则下列判断正确的是( )| A. | 最简单氢化物的稳定性:R>Q>X;R>T>X | |
| B. | 五种元素中Z的活动性最弱,T的氧化物对应水化合物酸性最强 | |
| C. | Q单质能从溶液中置换出X单质,R单质能从溶液中置换出T单质 | |
| D. | X阴离子和T阴离子相比,半径:X阴离子的大;还原性:T阴离子的强 |
14.煤炭燃烧中会产生大量烟气容易造成污染,用如图所示的电解池在较高温度下反应,可以净化烟气,则下列判断不正确的是( )


| A. | 据图可知,阳极反应式为2SO42--4e-=2SO3↑+O2↑ | |
| B. | 阳极失去2mol电子时,理论上可以得到11.2L氧气 | |
| C. | SO2在阴极与O2反应生成硫酸根,则方程式为SO2+O2+2e-=SO42- | |
| D. | CO2不参与电极反应,净化器中CO2浓度升高 |
11.含有6.02×1023个O原子的H2O2物质的量是( )
| A. | 1mol | B. | 0.5mol | C. | 0.25mol | D. | 0.125mol |
8. 回答以下问题:
回答以下问题:
(1)Ni(CO)4是无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂.推测Ni(CO)4是非极性分子(填“极性”或“非极性”).
(2)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ/mol.根据右表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子.
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.
①N2H4分子中含有极性键的数目是4;NH4+的空间构型是正四面体.
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=-1038.7kJ•mol-1若该反应中有8mol N-H键断裂,则形成的π键有6mol.
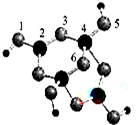
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
①在Xm-中,硼原子轨道的杂化类型有sp2杂化和sp3杂化;配位键存在于4号与5号原子之间(填原子的数字标号);m=2(填数字).
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有BCD(填序号).
A.共价键 B.离子键 C.氢键 D.范德华力 E.金属键.
 回答以下问题:
回答以下问题:(1)Ni(CO)4是无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂.推测Ni(CO)4是非极性分子(填“极性”或“非极性”).
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物.
①N2H4分子中含有极性键的数目是4;NH4+的空间构型是正四面体.
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=-1038.7kJ•mol-1若该反应中有8mol N-H键断裂,则形成的π键有6mol.
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
①在Xm-中,硼原子轨道的杂化类型有sp2杂化和sp3杂化;配位键存在于4号与5号原子之间(填原子的数字标号);m=2(填数字).
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有BCD(填序号).
A.共价键 B.离子键 C.氢键 D.范德华力 E.金属键.
12.下列各组中的两种物质在溶液中的反应,可用同一种离子方程式表示的是( )
| A. | 氧化铜分别溶于盐酸和醋酸 | |
| B. | 石灰石分别与硝酸和盐酸反应 | |
| C. | 硫酸铜溶液分别与氯化钡和氢氧化钡溶液反应 | |
| D. | 稀硫酸分别与碳酸钠、碳酸氢钠溶液反应 |