题目内容
下列实验能达到目的是( )
 |
 |
 |
 |
| A.检验SO2具有漂白性 | B.配制0.1mol?L-1NaOH溶液时定容 | C.分离出碘水中的碘 | D.配制一定浓度硫酸溶液 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.加热条件下浓硫酸和铜反应生成二氧化硫,二氧化硫可与品红褪色,可与碱溶液反应;
B.配制溶液时,视线应与液面水平相切;
C.乙醇与水混溶;
D.不能在容量瓶中稀释浓硫酸.
B.配制溶液时,视线应与液面水平相切;
C.乙醇与水混溶;
D.不能在容量瓶中稀释浓硫酸.
解答:
解:A.加热条件下浓硫酸和铜反应生成二氧化硫,二氧化硫可与品红褪色,可与碱溶液反应,可完成实验,故A正确;
B.配制溶液时,视线应与液面水平相切,仰视易导致浓度偏低,故B错误;
C.乙醇与水混溶,应用蒸馏的方法分离,故C错误;
D.容量瓶只能用于配制溶液,且在常温下使用,不能在容量瓶中稀释浓硫酸,故D错误.
故选A.
B.配制溶液时,视线应与液面水平相切,仰视易导致浓度偏低,故B错误;
C.乙醇与水混溶,应用蒸馏的方法分离,故C错误;
D.容量瓶只能用于配制溶液,且在常温下使用,不能在容量瓶中稀释浓硫酸,故D错误.
故选A.
点评:本题考查化学实验方案的评价,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
下表中列出了25℃、101kPa时一些物质的燃烧热数据
已知键能:C-H键:413.4kJ?mol-1、H-H键:436.0kJ?mol-1.则下列叙述正确的是( )
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ?mol-1 | 890.3 | 1299.6 | 285.8 |
| A、C≡C键能为796.0 kJ?mol-1 |
| B、C-H键键长小于H-H键 |
| C、2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ?mol-1 |
| D、2CH4(g)═C2H2(g)+3H2(g)△H=-376.4 kJ?mol-1 |
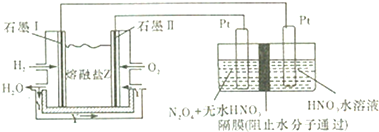
以H2、O2、熔融盐Na2CO3组成的燃料电池来电解制备N2O5,装置如图所示,其中Y为CO2.下列说法错误的是
( )
( )

| A、石墨Ⅱ电极上发生反应的电极反应式为:O2+4e-+2CO2═2CO32- |
| B、在电解池中生成N2O5的电极反应式为:N2O4+2NO3--2e-═2N2O5 |
| C、放电时熔融盐中CO32-向石墨I电极方向移动 |
| D、每消耗11.2L氢气,理论上可以制得108g N2O5 |
下列反应的离子方程式书写正确的是( )
| A、用食醋除去水壶内的水垢:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、FeBr2溶液中通入少量Cl2:2Br-+Cl2═Br2+2Cl- |
| D、在NaHCO3溶液中加入少量石灰水:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O |
下列离子或分子组能大量共存,且满足相应要求的是( )
| A、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即有气体产生 |
| C、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、30g SiO2含有NA个Si-O共价键 |
| B、1L 0.2mol?L-1 Al2(SO4)3溶液中的离子总数为NA |
| C、标准状况下,22.4L H2O所含原子个数大于3NA |
| D、含4mol HCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
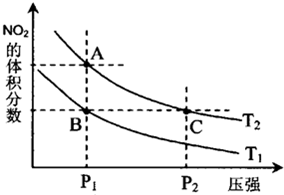 试运用所学知识,解决下列问题:
试运用所学知识,解决下列问题:

