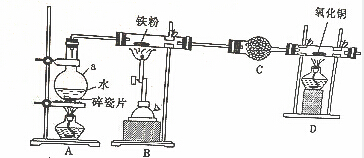
题目内容
8.有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、SO32-、OH-中的两种组成.它们具有下列性质:①A不溶于水和盐酸 ②B不溶于水但溶于盐酸并放出无刺激性气味的气体
③C的水溶液呈碱性,与H2SO4反应生成A
④D可溶于水,与H2SO4作用时放出的气体E可使溴水褪色.试回答以下问题
(1)推断A~E的化学式:A.BaSO4;B.BaCO3;C.Ba(OH)2;D.K2SO3;E.SO2.
(2)有关反应的离子方程式:
①B与盐酸反应2H++BaCO3=CO2↑+H2O+Ba2+,;②C与硫酸反应Ba2++2OH-+2H++SO42-═BaSO4+2H2O;
③D与硫酸反应SO32-+2H+═H20+SO2↑;④E与溴水反应2H20+SO2+Br2═4H++2Br--+SO42-.
分析 有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、SO32-、OH-组成,
①A不溶于水和盐酸,应为硫酸钡;
②B不溶于水但溶于盐酸,并放出无气味的气体,该气体可使澄清石灰水变浑浊,可知是BaCO3;
③C的水溶液呈碱性,与硫酸反应生成A,依据A为BaSO4分析,C为Ba(OH)2;
④D可溶于水,与H2SO4作用时放出气体E,E可使溴水褪色,D为K2SO3,以此解答该题.
解答 解:有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、SO32-、OH-组成,
①A不溶于水和盐酸,应为硫酸钡;
②B不溶于水但溶于盐酸,并放出无气味的气体,该气体可使澄清石灰水变浑浊,可知是BaCO3;
③C的水溶液呈碱性,与硫酸反应生成A,依据A为BaSO4分析,C为Ba(OH)2;
④D可溶于水,与H2SO4作用时放出气体E,E可使溴水褪色,D为K2SO3,
(1)上述推断得到A为BaSO4,B为BaCO3,C为Ba(OH)2 ,D为K2SO3,E为CO2,故答案为:BaSO4;BaCO3;Ba(OH)2;K2SO3;CO2;
(2)B与盐酸反应是BaCO3和盐酸反应生成氯化钡和水,反应的离子方程式为:2H++BaCO3=CO2↑+H2O+Ba2+,
C和硫酸反应是Ba(OH)2和硫酸反应生成硫酸钡和水,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,
D与硫酸反应是K2SO3和硫酸反应生成二氧化碳和水,反应的离子方程式为:SO32-+2H+═H20+SO2↑,
E(少量)与溴水反应生成氢溴酸和硫酸,反应的离子方程式为:2H20+SO2+Br2═4H++2 Br--+SO42-,
故答案为:2H++BaCO3=CO2↑+H2O+Ba2+;Ba2++2H++2OH-+SO42-=BaSO4↓+2H2O;SO32-+2H+═H20+SO2↑;2H20+SO2+Br2═4H++2 Br--+SO42-.
点评 本题考查了物质推断,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质性质和反应现象的分析判断,物质检验实验方法分析,实验过程中反应现象的理解应用,物质和离子性质熟练掌握是解题关键,题目难度中等.

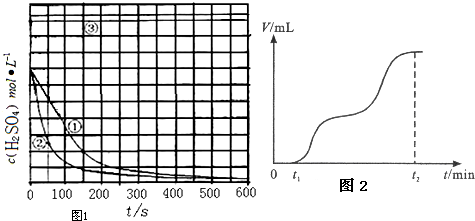
[实验设计]控制用同种铁块,初始使用硫酸体积均为1000mL,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验 编号 | 实验目的 | T/K | Fe/g | c(H2SO4)/mol•L-1 |
| ① | 为以下实验作参考 | 298 | 10 | 1.0 |
| ② | 探究温度对反应速率的影响 | |||
| ③ | 298 | 10 | 18.4 |
(2)实验①、②表明温度越高,反应速率越快
请再提出一种加快该反应速率的方法增大同质量铁的表面积或加入少量硫酸铜,构成原电池
(3)实验③得出的结论是:当硫酸浓度为18.4mol/L,反应速率趋向于零(反应速率趋向于停止),原因是常温下,铁与浓硫酸发生钝化
[思考与交流]
(4)实验③,若t1时开始加热,在铁的表面逐渐产生气泡,当有大量气泡产生时,控制反应温度基本不变.甲同学将收集到的气体体积与时间的关系粗略地表示为图2.t1~t2时间段,反应生成的气体是SO2、H2.写出开始加热时发生反应的化学方程式:2Fe+6H2SO4(浓)═Fe2(SO4)3+3SO2↑+6H2O.
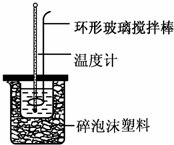 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是Cu传热快,热量损失大.
(2)在操作正确的前提下,提高中和热测定准确性的关键是提高装置的保温效果.大烧杯如不盖硬纸板,求得的中和热数值将偏小(填“偏大”、“偏小”或“无影响”).结合日常生活实际该实验在保温杯中(家用产品)效果更好.
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H=-56.8kJ/mol(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容C按4.18J•(g•℃)-1计算,结果保留小数点后一位).
(4)如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将偏大(填“偏大”、“偏小”、“不变”).如改用60mL0.5mol/L的盐酸与50mL 0.55mol•L-1的NaOH 溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等”或“不相等”),所求中和热相等(填“相等”或“不相等”).
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是ABDF(填字母序号).
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.
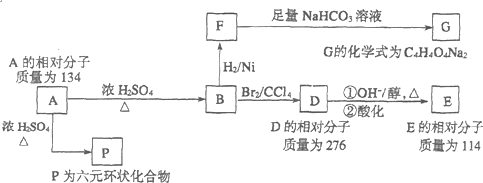
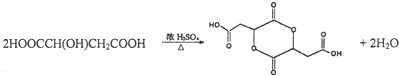 .
.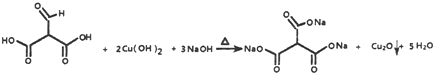 .
.
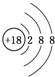 .元素K名称为氯在周期表中的位置第三周期第ⅦA族.
.元素K名称为氯在周期表中的位置第三周期第ⅦA族.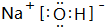
 HClO+HCl.
HClO+HCl.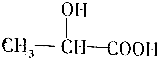 ,
,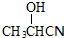 .
.