题目内容
对酸雨的pH描述中最准确的是( )
| A、小于7 |
| B、小于5.6 |
| C、在5.6~7之间 |
| D、等于5.6 |
考点:二氧化硫的污染及治理
专题:电离平衡与溶液的pH专题,元素及其化合物
分析:正常的雨水中溶解了二氧化碳,二氧化碳和水反应生成碳酸,碳酸电离导致溶液中氢离子浓度大于氢氧根离子浓度而使溶液呈酸性,正常雨水的pH为5.6,如果雨水溶解了二氧化硫、氮氧化物,会使溶液的酸性更强,据此进行解答.
解答:
解:雨水中由于溶解了二氧化碳而使正常雨水的pH=5.6,若雨水中溶解了二氧化硫或氮氧化物,使雨水变成亚硫酸或硝酸溶液,亚硫酸不稳定易被氧气氧化生成硫酸,硫酸和硝酸都是强酸,导致雨水的pH减小,小于5.6,
故选B.
故选B.
点评:本题考查了酸雨的pH大小,明确二氧化硫和氮氧化物是形成酸雨的主要物质是解本题的关键,注意:正常雨水因为溶解了二氧化碳而使其溶液的pH为5.6,不能误认为正常雨水的pH是7,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列除杂方法(括号内为杂质)操作正确的是( )
| A、乙醇(水)加新制的生石灰,过滤 |
| B、乙烷(乙烯)通过溴水溶液,洗气 |
| C、溴苯(苯)加水,振荡静置后分液 |
| D、乙酸乙酯(乙酸)加饱和NaHCO3溶液,振荡静置后蒸馏 |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 如图实验制取少量的Fe(OH)3胶体 |
B、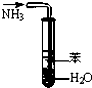 如图实验试管中溶液吸收NH3,并防止倒吸 |
C、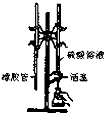 如图实验用H2SO4标准溶液滴定NaOH溶液 |
D、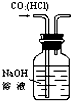 可用如图实验装置除去CO2气体中含有的少量HCl杂质 |
英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些孔洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织成的“笼子”,整体上看呈现出多孔特征,有些类似自然界中的蜂窝结构.下列有关说法正确的是( ) 

| A、该材料是一种特殊结构的金属 |
| B、该材料只吸收CO2,其他任何气体都能自由通过 |
| C、该材料吸收22.4LCO2后,增重44g |
| D、该材料可用于工厂的烟囱,吸收CO2,减少碳排放 |
常温下,现有溶液中溶质的物质的量浓度均为0.01mol?L-1的四种溶液:①盐酸,②硫酸,③醋酸,④NaOH,下列说法正确的是( )
| A、pH由小到大的顺序是①<②<③<④ |
| B、溶液中水电离出的H+浓度由小到大的顺序是②<①<④<③ |
| C、取一定体积的④溶液,分别和①、②、③溶液完全中和,消耗①、②、③溶液的体积由小到大的顺序是②<①<③ |
| D、取a体积的①溶液和b体积的④溶液混合后,溶液的pH为3,则a:b约为11:9 |


