题目内容
8.关于苯和苯酚的叙述中正确的是( )| A. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| B. | 在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色 | |
| C. | 苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸钠 | |
| D. | 实验时手指不小心沾上苯酚,立即用70℃以上的热水清洗 |
分析 A.实验室制取硝基苯时,首先滴加浓硝酸,然后向硝酸中逐滴滴加浓硫酸,最后加苯;
B.苯不溶于水,密度比水小;
C.苯酚酸性比碳酸弱,比碳酸氢钠强;
D.应防止烫伤.
解答 解:A.实验室制取硝基苯时,首先滴加浓硝酸,然后向硝酸中逐滴滴加浓硫酸,最后加苯,防止酸性飞溅且防止苯挥发,故A错误;
B.苯不溶于水,密度比水小,则在苯中加入酸性KMnO4溶液,振荡并静置后下层液体为紫色,故B正确;
C.苯酚酸性比碳酸弱,比碳酸氢钠强,苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸氢钠,故C错误;
D.应防止烫伤,苯酚易溶于酒精,可用酒精洗涤,故D错误.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,难度不大.

练习册系列答案
相关题目
11.下列说法错误的是( )
| A. | 重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 | |
| B. | Cu2+与足量氨水反应的离子方程式 Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ | |
| C. | 抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快 | |
| D. | 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 |
19.物质发生化学变化时:①电子总数②原子总数③分子总数④物质的种类⑤物质的总质量⑥物质的总能量,反应前后肯定不发生变化的是( )
| A. | ①②③⑤ | B. | ①②⑤ | C. | ②⑤⑥ | D. | ①④⑤⑥ |
16. 如图所示是探究铁发生腐蚀的装置图.发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升.下列说法不正确的是( )
如图所示是探究铁发生腐蚀的装置图.发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升.下列说法不正确的是( )
 如图所示是探究铁发生腐蚀的装置图.发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升.下列说法不正确的是( )
如图所示是探究铁发生腐蚀的装置图.发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升.下列说法不正确的是( )| A. | 两种腐蚀负极的电极反应式均为Fe-2e-═Fe2+ | |
| B. | 开始时发生的是析氢腐蚀 | |
| C. | 一段时间后发生的是吸氧腐蚀 | |
| D. | 析氢腐蚀的总反应式为2Fe+O2+2H2O═2Fe(OH)2 |
3.用NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
| A. | 常温下,4.48 L N2和O2的混合气体中所含原子数为0.4NA | |
| B. | 常温下,1.0 L 1.0 mol•L-1NaAlO2溶液中含有的氧原子数为2NA | |
| C. | 7.8 g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
| D. | 0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.2NA |
13.下列关于烷烃与烯烃的性质及反应类型的对比中正确的是( )
| A. | 烷烃只含有饱和键,烯烃只含有不饱和键 | |
| B. | 烷烃不能发生加成反应,烯烃只能发生加成反应 | |
| C. | 通式为CnH2n+2的一定是烷烃,通式为CnH2n的一定是烯烃 | |
| D. | 烷烃与烯烃相比,发生加成反应的一定是烯烃 |
17.A~F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如表所示.
请回答下列问题:
(1)A在元素周期表中的位置是第三周期第ⅡA族;A与E形成的化合物的电子式是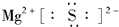 .
.
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是2Fe3++Cu═2Fe2++Cu2+.
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(4)F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 元素 | 原子结构或性质 |
| A | 原子最外层电子数是内层电子总数的$\frac{1}{5}$ |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)A在元素周期表中的位置是第三周期第ⅡA族;A与E形成的化合物的电子式是
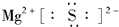 .
.(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是2Fe3++Cu═2Fe2++Cu2+.
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2.
(4)F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
18.下列各组离子在指定条件下能大量共存的是( )
| A. | 通入氯气:K+、Fe2+、SO42-、Br- | |
| B. | 通入SO2:Ba2+、NH4+、NO3-、Cl- | |
| C. | 加入氧化钠固体:Mg2+、HCO3-、SO42- | |
| D. | 透明溶液中:Cu2+、Fe3+、NO3-、Cl- |
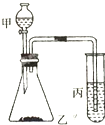 比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实
比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实