题目内容
X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收.已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应.请根据叙述完成下列问题:
(1)写出下列物质的化学式:X ;Y ;Z .
(2)写出有关反应的化学方程式:
X在一定条件下与氧气的反应: .
Z与水反应的方程式为 .
(1)写出下列物质的化学式:X
(2)写出有关反应的化学方程式:
X在一定条件下与氧气的反应:
Z与水反应的方程式为
考点:无机物的推断
专题:推断题
分析:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收,说明这三种气体能和碱反应,X是化石燃料燃烧的产物之一,是形成酸雨的主要物质,化石中含有S元素,二氧化硫和氮氧化物是酸性酸雨的主要气体,所以X是SO2;Y是一种单质,它的水溶液具有漂白作用,氯气和水反应生成的次氯酸具有漂白性,且氯气有毒,所以Y是Cl2;Z是硝酸工业和汽车尾气中的有害物质之一,汽车尾气中含有一氧化氮和二氧化氮,能与水反应的氮氧化物是二氧化氮,则Z是NO2,以此来解答.
解答:
解:(1)X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收,说明这三种气体能和碱反应,X是化石燃料燃烧的产物之一,是形成酸雨的主要物质,化石中含有S元素,二氧化硫和氮氧化物是酸性酸雨的主要气体,所以X是SO2;Y是一种单质,它的水溶液具有漂白作用,氯气和水反应生成的次氯酸具有漂白性,且氯气有毒,所以Y是Cl2;Z是硝酸工业和汽车尾气中的有害物质之一,汽车尾气中含有一氧化氮和二氧化氮,能与水反应的氮氧化物是二氧化氮,则Z是NO2,
故答案为:SO2;Cl2;NO2;
(2)X是二氧化硫,在催化剂、加热条件下,二氧化硫和氧气反应生成三氧化硫,反应方程式为2SO2+O2
2SO3,
Z和水反应生成硝酸和一氧化氮,反应方程式为3NO2+H2O=2HNO3+NO,
故答案为:2SO2+O2
2SO3;3NO2+H2O=2HNO3+NO.
故答案为:SO2;Cl2;NO2;
(2)X是二氧化硫,在催化剂、加热条件下,二氧化硫和氧气反应生成三氧化硫,反应方程式为2SO2+O2
| 催化剂 |
| △ |
Z和水反应生成硝酸和一氧化氮,反应方程式为3NO2+H2O=2HNO3+NO,
故答案为:2SO2+O2
| 催化剂 |
| △ |
点评:本题考查无机物的推断,为高频考点,注意物质的性质(毒性、溶解性、化学性质)的应用,明确形成酸雨的气体及汽车尾气、漂白性为解答的关键,侧重N、S化合物性质的考查,题目难度不大.

练习册系列答案
相关题目
在恒温恒容条件下,将4molA和2molB放入一密闭容器中2A(g)+B(g)?2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )
| A、4mol、2mol、0mol、2mol |
| B、2mol、1mol、2mol、2mol |
| C、2mol、1mol、2mol、1mol |
| D、2mol、1mol、0mol、1mol |
既能使石蕊试液变红,又能使品红试液变为无色,还能使溴水褪色的是( )
| A、Cl2 |
| B、HCl |
| C、SO2 |
| D、CO2 |
某化合物由碳、氢、氧三种元素组成,其红外光谱图有C-H键、H-O键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式可能是( )
| A、CH3CH2CH2OH |
B、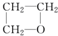 |
| C、CH3CH2OCH3 |
| D、CH3CH2CHO |
 粗镍经过下列过程可以转化为纯度99.9%的高纯镍,管状反应装置如图.
粗镍经过下列过程可以转化为纯度99.9%的高纯镍,管状反应装置如图.管中发生的反应是Ni(s)+4CO(g)
| 50℃-180℃ |
| 180℃-200℃ |
下列说法不正确的是( )
| A、反应管粗镍端为低温区,高纯镍端为高温区 |
| B、该反应体系在一定条件下达到平衡状态的标志之一是体系的压强不变 |
| C、提纯过程中,CO会逐渐减少 |
| D、该装置可用于碘的提纯 |
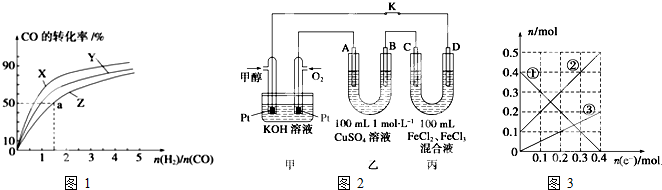
 认真读书,回归课本,请回答下列问题:
认真读书,回归课本,请回答下列问题: