题目内容
A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05mol在0.125mol的氧气中恰好完全燃烧,生成0.1molCO2和0.1molH2O.试通过计算回答:取a mol 以任意物质的量比混合的A和B的混合物,在过量的氧气中完全燃烧.
①若耗氧量为定值,则耗氧量为 mol(用含a的代数式表示)
②若耗氧量一定,则A、B的分子式分别是 、
③若生成的二氧化碳和水的物质的量一定,则A、B的分子式分别是 、
①若耗氧量为定值,则耗氧量为
②若耗氧量一定,则A、B的分子式分别是
③若生成的二氧化碳和水的物质的量一定,则A、B的分子式分别是
考点:有关混合物反应的计算
专题:
分析:由A和B的混合物0.05mol在0.125mol的氧气中完全燃烧生成0.1 molCO2和0.1molH2O,则0.05mol有机物混合物中含有氧原子物质的量为0.1mol×2+0.1mol-0.125mol×2=0.05mol,可知A和B的混合物平均组成分子式为C2H4O,由于A为烃,B为烃的含氧衍生物,且A和B为等物质的量,根据平均值含义(如A与B中碳原子数确定,有两种可能:一种情况是两者碳原子数均为2;另一情况是一种碳原子数大于2,一种碳原子数小于2),A、B的组合可能有五种.分别是CH4和C3H4O2、C2H4和C2H4O2、C2H2和C2H6O2、C2H6和C2H2O2、C3H6和CH2O2;
①②由于A为烃,B为烃的含氧衍生物,则B中必含2个O原子,将其以任意物质的量比混合,且物质的量之和一定时,两者碳原子数均为2,且组成中(x+
-
)相等,A、B以任意物质的量比混合,且物质的量之和一定时,两者碳原子数均为2,耗氧量一定,则为CH≡CH和 ,然后假定全为乙炔进行计算耗氧量;
,然后假定全为乙炔进行计算耗氧量;
③若生成的CO2 和 H2O 的物质的量一定,则两种物质中含有的C和H原子数分别相同.
①②由于A为烃,B为烃的含氧衍生物,则B中必含2个O原子,将其以任意物质的量比混合,且物质的量之和一定时,两者碳原子数均为2,且组成中(x+
| y |
| 4 |
| z |
| 2 |
 ,然后假定全为乙炔进行计算耗氧量;
,然后假定全为乙炔进行计算耗氧量;③若生成的CO2 和 H2O 的物质的量一定,则两种物质中含有的C和H原子数分别相同.
解答:
解:由A和B的混合物0.05 mol燃烧生成0.1 mol CO2和0.1 mol H2O以及耗氧量,可知A和B的混合物平均组成分子式为C2H4O,由于A为烃,B为烃的含氧衍生物,且A和B为等物质的量,根据平均值含义(如A与B中碳原子数确定,有两种可能:一种情况是两者碳原子数均为2;另一情况是一种碳原子数大于2,一种碳原子数小于2),A、B的组合可能有五种,
根据题意,A和B以任意比混合,①耗氧量一定,则A和B耗氧能力相同,即A为C2H2,B为C2H6O2〔C2H2(H2O)2〕,耗氧量为2.5a mol,
故答案为:2.5a;
②根据①可知,A、B的分子式分别为:C2H2,C2H6O2,
故答案为:C2H2;C2H6O2;
②生成CO2和H2O的物质的量一定,则A、B两物质中C、H原子数分别相同,即A为C2H4、B为C2H4O2;
故答案为:C2H4、C2H4O2.
| 一 | 二 | 三 | 四 | 五 | |
| A | CH4 | C2H2 | C2H4 | C2H6 | C3H6 |
| B | C3H4O2 | C2H6O2 | C2H4O2 | C2H2O2 | CH2O2 |
故答案为:2.5a;
②根据①可知,A、B的分子式分别为:C2H2,C2H6O2,
故答案为:C2H2;C2H6O2;
②生成CO2和H2O的物质的量一定,则A、B两物质中C、H原子数分别相同,即A为C2H4、B为C2H4O2;
故答案为:C2H4、C2H4O2.
点评:本题考查了有机物分子式的计算,题目难度中等,注意掌握有机物燃烧通式及其应用方法,明确确定有机物分子式、结构简式的方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度,有关叙述正确的是( )
| A、H2Y在电离时:H2Y+H2O?HY-+H3O+ |
| B、在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+) |
| C、在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
| D、HY-水解方程式为:HY-+H2O?Y2-+H3O+ |
容量瓶上必须标明( )
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
①温度 ②浓度 ③容量 ④压强 ⑤刻度线.
| A、②③④ | B、①③⑤ | C、③④ | D、③ |
今有室温下四种溶液,有关叙述不正确的是( )
| ① | ② | ③ | ④ | |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| A、①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小 |
| B、分别加水稀释10倍,四种溶液的pH:①>②>④>③ |
| C、①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、VaL④与VbL②溶液混合后,若混合后溶液pH=7,则Va:Vb=1:11 |
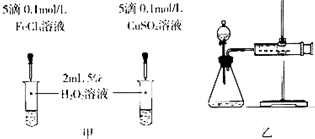
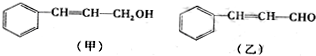 丙
丙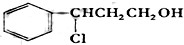
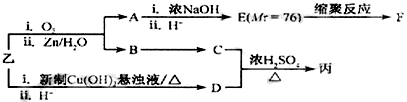
 乙酸是生活中的一种常见有机物,它的分子结构模型如图所示.
乙酸是生活中的一种常见有机物,它的分子结构模型如图所示.