题目内容
20.如图中A至F是化合物,G是单质.A,B,E,F的焰色均是黄色.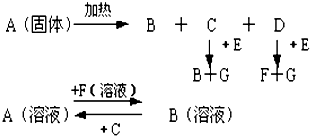
写出A、B、E、F的化学式:
ANaHCO3,BNa2CO3,ENa2O2,FNaOH.
分析 A至F是化合物,G是单质,A、B、E、F的焰色均是黄色,说明A、B、E、F都含有Na元素,A固体受热分解生成三种物质,则A为NaHCO3,B为Na2CO3,CO2和H2O都能和Na2O2反应生成钠的化合物和O2,G是单质,则G是O2,C和E反应生成Na2CO3,则C是CO2,所以D为H2O,E为Na2O2,NaHCO3和F反应生成Na2CO3,F为NaOH,据此分析解答.
解答 解:A至F是化合物,G是单质,A、B、E、F的焰色均是黄色,说明A、B、E、F都含有Na元素,A固体受热分解生成三种物质,则A为NaHCO3,B为Na2CO3,CO2和H2O都能和Na2O2反应生成钠的化合物和O2,G是单质,则G是O2,C和E反应生成Na2CO3,则C是CO2,所以D为H2O,E为Na2O2,NaHCO3和F反应生成Na2CO3,F为NaOH,
通过以上分析知,A、B、E、F分别是NaHCO3、Na2CO3、Na2O2、NaOH,
故答案为:NaHCO3;Na2CO3;Na2O2;NaOH.
点评 本题考查无机物推断,为高频考点,侧重考查学生分析推断能力,明确物质性质及物质之间的转化是解本题关键,以焰色反应为突破口进行推断,题目难度不大.

练习册系列答案
相关题目
10.下列有关仪器的使用方法、实验操作或实验结果正确的是( )
| A. | 洗净的锥形瓶和容量瓶可以放进烘箱中烘干 | |
| B. | 酸式滴定管装标准液前,不需用该标准溶液润洗 | |
| C. | 锥形瓶用作反应容器时一定不能加热 | |
| D. | 蒸馏时若温度计水银球的位置低于蒸馏烧瓶支管口,可能会导致产品中混有低沸点杂质 |
11.1-18号元素中某核素A的阳离子An+核外共有X个 电子,则核素A的最外层电子数为( )
| A. | x+n | B. | x-n | C. | n | D. | n+2 |
8.2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖.青蒿素分子式C15H22O5,相对分子质量为282.下面关于青蒿素的说法正确的是( )
| A. | 1 mol C15H22O5的质量为282g/mol | |
| B. | C15H22O5的摩尔质量等于它的相对分子质量 | |
| C. | 一个C15H22O5微粒的质量约为 $\frac{282}{6.02×1{0}^{23}}$g | |
| D. | 含有6.02×1023个碳原子的C15H22O5的物质的量为1 mol |
15.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.1mol NaOH中含有的阴离子数目为0.1NA | |
| B. | 1L 0.05mol•L-1CH3COOH溶液中含有的H+数目为0.05NA | |
| C. | 标准情况下,44.8L CCl4含有的分子数为2NA | |
| D. | 反应:ClO2-+5Cl-+6H+═3Cl2+3H2O中,每生成1mol Cl2,转移的电子数为2NA |
4.已知反应2N2O5(g)?4NO2(g)+O2(g)的分解速率表达式为v正=k正.cm(N2O5),k正是与温度有关的常数,340K时实验测得的有关数据如下:
下列有关叙述不正确的是( )
| t/min | 1 | 2 | 3 | 4 |
| c(N2O5)/mol.L-1 | 0.133 | 0.080 | 0.057 | 0.040 |
| v正/mol.L-1.min-1 | 0.0466 | 0.028 | 0.020 | 0.014 |
| A. | 340K时,速率表达式中m=1 | |
| B. | 340K时,速率表达式中k正≈0.35min-1 | |
| C. | 340K时,若c(N2O3)=0.100mol.L-1,则v正≈0.035mol.L-1.min-1 | |
| D. | 若t=2min时升高温度,则m不变,k正减小 |
2.下列说法错误的是( )
| A. | 化学反应中的能量变化都表现为热量变化 | |
| B. | 需要加热才能发生的反应不一定是吸热反应 | |
| C. | 任何化学反应过程中都伴随有能量的变化 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |