题目内容
7.下列关于有机化合物的说法正确的是( )| A. | 乙醇和乙酸都能与金属钠反应 | |
| B. | 用氢氧化钠除去乙酸乙酯中的少量乙酸 | |
| C. | 植物油和动物脂肪都不能使溴水褪色 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
分析 A.乙醇含-OH、乙酸含-COOH;
B.乙酸乙酯、乙酸均与NaOH反应;
C.植物油中含碳碳双键;
D.乙烯含碳碳双键,聚乙烯不含.
解答 解:A.乙醇含-OH、乙酸含-COOH,均与Na反应生成氢气,故A正确;
B.乙酸乙酯、乙酸均与NaOH反应,不能除杂,应选饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸,故B错误;
C.植物油中含碳碳双键,能使溴水褪色,而动物脂肪不能,故C错误;
D.乙烯含碳碳双键,能使溴的四氯化碳溶液褪色,而聚乙烯不能,故D错误;
故选A.
点评 本题考查有机物结构和性质,为高频考点,把握官能团与性质的关系是解本题关键,侧重分析与应用能力的考查,注意常见有机物的性质及混合物分离提纯,题目难度不大.

练习册系列答案
相关题目
17.常温下,将某一元酸HA溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
(1)在①组实验中0.1mol•L-1HA溶液中水的电离程度为a,0.1mol•L-1NaOH溶液中水的电离程度为b,所得混合溶液中水的电离程度为c.则a、b、c由大到小的顺序是cab.
(2)在②组实验中c>0.2(填“<”、“>”或“=”).
(3)根据③组实验所得的混合溶液,其溶液中离子浓度大小排列顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
(4)常温下,已知KSP[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于5.
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(2)在②组实验中c>0.2(填“<”、“>”或“=”).
(3)根据③组实验所得的混合溶液,其溶液中离子浓度大小排列顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
(4)常温下,已知KSP[Cu(OH)2]=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol•L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于5.
18.下列关于元素周期表的叙述正确的是( )
| A. | 元素周期表中有七行,七个周期,有18列,18个族 | |
| B. | 目前使用的元素周期表中,同一主族的元素最外层电子数相同 | |
| C. | 短周期元素是指1~20号元素,其中大多数为非金属 | |
| D. | 元素周期表中,元素的种数与对应的原子种数一样多 |
16.下列离子方程式书写正确的是( )
| A. | 铜和稀硝酸反应 Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| B. | 碳酸氢钠的水解 HCO3-+H2O?CO32-+H3O+ | |
| C. | Fe投入盐酸中 2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氢氧化铝溶于氢氧化钠溶液 Al(OH)3+OH-=AlO2-+2H2O |
17.石墨和金刚石都是碳元素的单质,石墨在一定条件下可转化为金刚石.已知12g石墨完全转化成金刚石时,要吸收E kJ的能量,下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石不如石墨稳定 | |
| C. | 等质量的石墨与金刚石完全燃烧,金刚石放出的能量少 | |
| D. | 等质量的石墨与金刚石完全燃烧,二者放出的热量相等 |
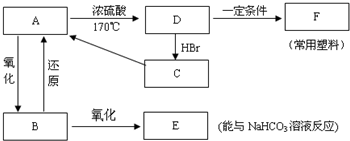
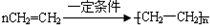 .
.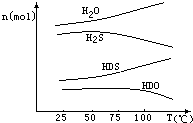 我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有:
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有: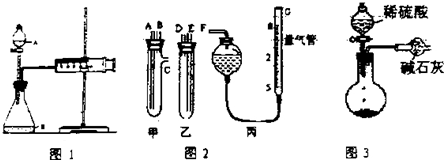
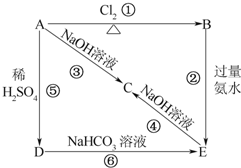 图示中,E是不溶于水的白色胶状物质.
图示中,E是不溶于水的白色胶状物质.