题目内容
2. 我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有:
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有:(1)空气吹出纯碱吸收法.方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到单质溴.该方法涉及的反应有:
①Cl2+2Br-=Br2+2Cl- (写出离子方程式);
②3Br2+3CO32-═BrO3-+5Br-+3CO2↑;
③BrO3-+5Br-+6H+═3Br2+3H2O (写出离子方程式);
(2)空气吹出SO2吸收法.该方法基本同(1),只是将吹出的溴用SO2溶液来吸收,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴.写出溴与二氧化硫反应的化学方程式Br2+SO2+2H2O=H2SO4+2HBr.
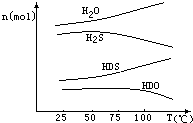
(3)海水中的氘(含HDO 0.03‰)发生聚变的能量,足以保证人类上亿年的能源消费,工业上可采用“硫化氢-水双温交换法”富集HDO.其原理是利用H2S、HDS、H2O和HDO四种物质,在25℃和100℃两种不同温度下发生的两个不同反应得到较高浓度的HDO.如图为“硫化氢-水双温交换法”所发生的两个反应中涉及的四种物质在反应体系中的物质的量随温度的变化曲线.写出100℃时所发生的反应的化学方程式H2S+HDO=HDS+H2O;工业上富集HDO的生产过程中,可以循环利用的一种物质是H2S.
分析 (1)①依据题干叙述可知氯气和溴化钠可以置换出溴单质,其化学化学方程式为:Cl2+2NaBr=2NaCl+Br2;
③溴离子和溴酸根离子用硫酸酸反应,发生氧化还原反应生成单质溴;
(2)溴有氧化性,二氧化硫有还原性,溴与二氧化硫在水溶液中发生氧化还原反应是硫酸和溴化氢;
(3)图象分析,物质的量减少的是反应物,增加的是生成物;HDS中的氢原子可以继续与HDO反应,故H2S可循环利用.
解答 解:(1)①依据题干叙述可知氯气和溴化钠可以置换出溴单质,其化学化学方程式为:Cl2+2NaBr=2NaCl+Br2,离子方程式为:Cl2+2Br-=Br2+2Cl-,
故答案为:Cl2+2Br-=Br2+2Cl-;
②溴离子和溴酸根离子用硫酸酸反应,发生氧化还原反应生成单质溴,反应的离子方程式为:BrO3--+5Br-+6H+═3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+═3Br2+3H2O;
(2)溴有氧化性,二氧化硫有还原性,在水溶液里,二氧化硫和溴发生氧化还原反应生成硫酸和氢溴酸,反应的离子方程式为:Br2+SO2+2H2O=H2SO4+2HBr,
故答案为:Br2+SO2+2H2O=H2SO4+2HBr;
(3)物质的量减少的是反应物,增加的是生成物,反应物为H2S,HDO,生成物为HDS,H2O;HDS中的氢原子可以继续与HDO反应,故H2S可循环利用,
故答案为:H2S+HDO=HDS+H2O; H2S.
点评 本题考查海水资源的提取原理、氧化还原反应等知识,注意离子方程式书写,掌握基础,仔细审题是解题关键,题目难度中等.

练习册系列答案
相关题目
12.下列说法中正确的是( )
| A. | 乙醇和乙二醇属于同系物 | |
| B. | 1-丁烯存在顺反异构体 | |
| C. | 将苯加入溴水中,溴水褪色,是因为发生了加成反应 | |
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
10.某粒子用${\;}_{Z}^{A}$Rn-表示,下列关于该粒子的叙述正确的是( )
| A. | 所含质子数=Z-n | B. | 所含中子数=A-Z+n | ||
| C. | 质量数=A+n | D. | 所含电子数=Z+n |
7.下列关于有机化合物的说法正确的是( )
| A. | 乙醇和乙酸都能与金属钠反应 | |
| B. | 用氢氧化钠除去乙酸乙酯中的少量乙酸 | |
| C. | 植物油和动物脂肪都不能使溴水褪色 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
14.下列实验或现象中,可证明胶体粒子带电荷的是( )
| A. | 电泳 | B. | 丁达尔效应 | C. | 布朗运动 | D. | 渗析 |
11.向纯水中加入少量NaHSO4固体,当温度不变时,则该溶液中( )
| A. | 水电离出的c(H+) 减小 | B. | c(OH-) 与 c(H+) 的乘积增大 | ||
| C. | c(H+ ) 减小 | D. | c(OH-) 增大 |
12.下列各项中表达正确的是( )
| A. | 次氟酸的结构式为H-F-O | B. | CH4分子的球棍模型: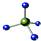 | ||
| C. | 1H、3H2、D互为同位素 | D. | CO2电子式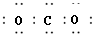 |

 ,A分子内含有的官能团是(填名称)醛基.
,A分子内含有的官能团是(填名称)醛基.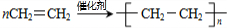 .
. 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示: