题目内容
【题目】已知某二元酸H2A在溶液中存在如下电离:H2A=H++HAˉ,HAˉ![]() H++A2ˉ,K=1.2×10-2。设NA为阿伏加德罗常数值。关于常温下0.01mol·L-1的H2A溶液,下列说法正确的是
H++A2ˉ,K=1.2×10-2。设NA为阿伏加德罗常数值。关于常温下0.01mol·L-1的H2A溶液,下列说法正确的是
A.![]()
B.pH<2
C.c(H+)=2c(H2A)+c(HAˉ)+c(OHˉ)
D.1L溶液中的H+数目为0.02NA
【答案】B
【解析】
A.![]() ,根据题意可知H2A第一步完全电离,第二步部分电离,所以0.01mol·L-1的H2A溶液中c(H+)>0.01mol/L,K=1.2×10-2,所以
,根据题意可知H2A第一步完全电离,第二步部分电离,所以0.01mol·L-1的H2A溶液中c(H+)>0.01mol/L,K=1.2×10-2,所以![]() <1.2,故A错误;
<1.2,故A错误;
B.H2A第一步完全电离,第二步部分电离,所以0.01mol·L-1的H2A溶液中c(H+)>0.01mol/L,则溶液的pH小于2,故B正确;
C.由于第一步完全电离,所以溶液中并不存在H2A,故C错误;
D.H2A第一步完全电离,第二步部分电离,所以0.01mol·L-1的H2A溶液中0.01mol/L<c(H+)<0.02mol/L,则1L该溶液中氢离子数目小于0.02NA,故D错误;
答案为B。

练习册系列答案
相关题目
【题目】按如图装置进行实验,下列推断正确的是( )
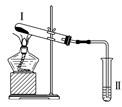
选项 | Ⅰ中试剂 | Ⅱ中试剂及现象 | 推断 |
A | 氯化铵 | 酚酞溶液不变红色 | 氯化铵稳定 |
B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成FeO和SO2 |
C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液褪色 | 石蜡油发生了化学变化 |
D | 铁粉与水蒸气 | 肥皂水冒泡 | 铁粉与水蒸气发生了反应 |
A. A B. B C. C D. D