题目内容
为了测定草酸晶体(H2C2O4?xH2O)中的x值,进行如下实验:
①称取W g草酸晶体,配成100.00mL溶液.
②取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4,用a mol/L KMnO4溶液滴定.
试回答:
(1)写出滴定过程中反应的化学方程式: .
(2)实验中,标准液KMnO4应装在 (填“酸式”或“碱式”)滴定管中.滴定终点时溶液由 色变为 色,且在30s内颜色不再恢复为原来颜色.
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x值会 (填“偏大”、“偏小”或“无影响”).
(4)在滴定过程中若用去a mol/L KMnO4溶液V mL,则所配制的草酸溶液的物质的量浓度为 mol/L,由此x= .
(5)若滴定终点读数时俯视,则计算的x值会 (填“偏大”、“偏小”或“无影响”).
①称取W g草酸晶体,配成100.00mL溶液.
②取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4,用a mol/L KMnO4溶液滴定.
试回答:
(1)写出滴定过程中反应的化学方程式:
(2)实验中,标准液KMnO4应装在
(3)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x值会
(4)在滴定过程中若用去a mol/L KMnO4溶液V mL,则所配制的草酸溶液的物质的量浓度为
(5)若滴定终点读数时俯视,则计算的x值会
考点:探究物质的组成或测量物质的含量,中和滴定
专题:实验探究和数据处理题
分析:实验有两个过程:为了配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;
用高锰酸钾溶液进行滴定测草酸的物质的量;
(1)草酸晶体滴入酸性高锰酸钾溶液发生氧化还原反应,2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
(2)高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,滴定终点时溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
(3)滴定时为减小实验误差,应用少量蒸馏水将锥形瓶内壁冲洗;
(4)令草酸的浓度为cmol/L,根据反应方程式计算;
根据草酸的质量计算水的质量,结合关系式H2C2O4?xH2O~H2C2O4 ~xH2O计算x的值;
(5)滴定终点时俯视滴定管刻度,会导致测量体积偏小,测定草酸质量偏小,则x值会偏大.
用高锰酸钾溶液进行滴定测草酸的物质的量;
(1)草酸晶体滴入酸性高锰酸钾溶液发生氧化还原反应,2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
(2)高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,滴定终点时溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
(3)滴定时为减小实验误差,应用少量蒸馏水将锥形瓶内壁冲洗;
(4)令草酸的浓度为cmol/L,根据反应方程式计算;
根据草酸的质量计算水的质量,结合关系式H2C2O4?xH2O~H2C2O4 ~xH2O计算x的值;
(5)滴定终点时俯视滴定管刻度,会导致测量体积偏小,测定草酸质量偏小,则x值会偏大.
解答:
解:为了配制准确浓度的草酸溶液,所需要的实验仪器主要有天平(含砝码)、烧杯、药匙、100mL容量瓶、胶头滴管、玻璃棒等;
用高锰酸钾溶液进行滴定测草酸的物质的量,
(1)草酸晶体滴入酸性高锰酸钾溶液发生氧化还原反应,反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
故答案为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
(2)高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,滴定终点时,溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
故答案为:酸;无,紫;
(3)滴定时为减小实验误差,应用少量蒸馏水将锥形瓶内壁冲洗,使草酸完全反应,所以用少量蒸馏水将锥形瓶内壁冲洗一下,对实验结果无影响,
故答案为:无影响;
(4)KMnO4 ~5H2C2O4
2mol 5mol
aV×10-3mol 0.025L×cmol/L
解得:c=0.1aVmol?L-1
H2C2O4?xH2O~H2C2O4 ~xH2O
1mol 18xg
0.1aV×0.1 w-0.1aV×0.1×90
解得x=
-5,
故答案为:0.1aV;
-5;
(5)滴定终点时俯视滴定管刻度,会导致测量体积偏小,测定草酸质量偏小,则x值会偏大,
故答案为:偏大.
用高锰酸钾溶液进行滴定测草酸的物质的量,
(1)草酸晶体滴入酸性高锰酸钾溶液发生氧化还原反应,反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
故答案为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O;
(2)高锰酸钾具有强氧化性,会腐蚀橡胶管,应装在酸式滴定管中,滴定终点时,溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
故答案为:酸;无,紫;
(3)滴定时为减小实验误差,应用少量蒸馏水将锥形瓶内壁冲洗,使草酸完全反应,所以用少量蒸馏水将锥形瓶内壁冲洗一下,对实验结果无影响,
故答案为:无影响;
(4)KMnO4 ~5H2C2O4
2mol 5mol
aV×10-3mol 0.025L×cmol/L
解得:c=0.1aVmol?L-1
H2C2O4?xH2O~H2C2O4 ~xH2O
1mol 18xg
0.1aV×0.1 w-0.1aV×0.1×90
解得x=
| 50w |
| 9av |
故答案为:0.1aV;
| 50w |
| 9av |
(5)滴定终点时俯视滴定管刻度,会导致测量体积偏小,测定草酸质量偏小,则x值会偏大,
故答案为:偏大.
点评:本题考查一定物质的量浓度溶液配制、滴定操作、滴定应用与计算、物质组成含量测定等,难度中等,注意滴定中经常根据关系式进行计算,掌握根据关系式计算方法.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列说法正确的是( )
| A、可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率 |
| B、S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子 |
| C、氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱 |
| D、Fe3+ 比Fe2+稳定,因为Fe3+价电子构型是3d5,d亚层处于半充满状态,稳定 |
四种短周期元素的性质或结构信息如下表.下列推断错误的是( )
| 元素编号 | 元素性质或结构 |
| T | M层上有2对成对电子 |
| X | 元素最高正价是+7价 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | 单质是银白色固体、导电、密度比水小,与水剧烈反应、和氧气反应不同条件下产物不同 |
| A、离子半径从小到大的顺序:Y<Z<T<X |
| B、X、Y形成化合物的晶体类型与X、Z形成化合物的晶体类型不同 |
| C、T的氢化物是同族元素氢化物中沸点最低的 |
| D、X的最高价氧化物对应的水化物是无机含氧酸中的最强酸 |
下列说法中,正确的是( )
| A、石油的主要成分是烃,煤经过分馏可制得焦炭、煤焦油等产品 |
| B、棉花、麻、蚕丝在一定条件下都能发生水解反应,主要成分是纤维素 |
| C、乙酸和乙醇可以发生酯化反应又都可以与钠发生置换反应 |
| D、乙烯和苯均能使溴水退色,都发生了加成反应 |
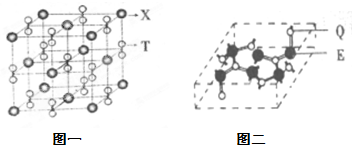 有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z.E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体.x为周期表前四周期中电负性最小的元素,Z的原子序数为28.
有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z.E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体.x为周期表前四周期中电负性最小的元素,Z的原子序数为28.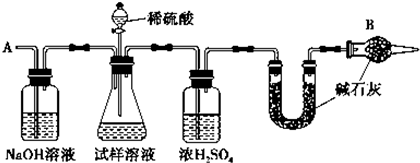
 烯烃A在一定条件下可以按如图进行反应.
烯烃A在一定条件下可以按如图进行反应.