题目内容
下列说法正确的是( )
| A、可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率 |
| B、S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子 |
| C、氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱 |
| D、Fe3+ 比Fe2+稳定,因为Fe3+价电子构型是3d5,d亚层处于半充满状态,稳定 |
考点:原子核外电子排布,元素周期律的作用,化学反应速率的影响因素
专题:
分析:A、升高温度,反应的活化能不变,活化分子百分数增大,加快反应速率;
B、电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形;
C、氮原子2p能级半充满,所以比较稳定,难以失去电子;
D、轨道处于半充满或全充满状态,较稳定.
B、电子云就是用小黑点疏密来表示空间各电子出现概率大小的一种图形;
C、氮原子2p能级半充满,所以比较稳定,难以失去电子;
D、轨道处于半充满或全充满状态,较稳定.
解答:
解:A、可逆反应在其他条件不变时,升高温度,反应的活化能不变,活化分子百分数增大,加快反应速率,故A错误;
B、S电子云是球形对称的,P电子云是纺锤形,电子云中小黑点本身没有意义,不代表1个电子,也不代表出现次数,故B错误;
C、氮原子2p能级半充满,所以比较稳定,氮原子的第一电离能大于氧原子,故C错误;
D、Fe3+价电子构型是3d5,Fe2+价电子构型是3d6,d亚层处于半充满状态,较稳定,所以Fe3+ 比Fe2+稳定,故D正确;
故选D.
B、S电子云是球形对称的,P电子云是纺锤形,电子云中小黑点本身没有意义,不代表1个电子,也不代表出现次数,故B错误;
C、氮原子2p能级半充满,所以比较稳定,氮原子的第一电离能大于氧原子,故C错误;
D、Fe3+价电子构型是3d5,Fe2+价电子构型是3d6,d亚层处于半充满状态,较稳定,所以Fe3+ 比Fe2+稳定,故D正确;
故选D.
点评:本题主要考查原子核外电子运动与排布,题目难度不大,本题注意知识的积累.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
 如图是部分被污损的某白色固体药品标签.为探究其成分,取样滴入适量盐酸,无气泡产生.则该固体( )
如图是部分被污损的某白色固体药品标签.为探究其成分,取样滴入适量盐酸,无气泡产生.则该固体( )| A、一定是NaCl |
| B、一定是NaNO3 |
| C、可能是Na2CO3 |
| D、可能是Na2SO4 |
下列各项中表达正确的是( )
A、F原子结构示意图: |
B、次氯酸电子式: |
| C、H、D、T表示同一种核素 |
D、CH4分子的球棍模型: |
物质的量相等的Na2CO3和 NaHCO3分别与足量的盐酸反应,得到CO2的物质的量之比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、1:3 |
下列离子方程式正确的是( )
| A、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C、石灰水与碳酸钠溶液混合:Ca2++CO32-=CaCO3↓ |
| D、硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图.关于该过程的相关叙述不正确的是( )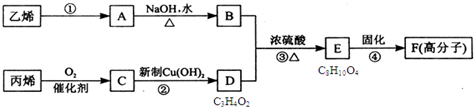

| A、反应④的反应类型是加聚 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1mol物质E最多可以消耗2molNaOH |