题目内容
铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
| A、9.02 g |
| B、8.51 g |
| C、8.26 g |
| D、7.04 g |
考点:有关混合物反应的计算
专题:
分析:最终生成沉淀为Cu(OH)2和Mg(OH)2,根据电荷守恒可知,金属失去电子物质的量等于沉淀中氢氧根的物质的量,根据电子转移守恒计算金属失去电子物质的量,沉淀质量等于金属质量与氢氧根离子质量之和.
解答:
解:4.48L的 NO2气体的物质的量为
=0.2mol,0.336L的N2O4气体物质的量为
=0.015mol,根据电子转移守恒,金属失去电子物质的量0.2mol×1+0.015mol×2×1=0.23mol,
最终生成沉淀为Cu(OH)2和Mg(OH)2,根据电荷守恒可知,金属失去电子物质的量等于沉淀中氢氧根的物质的量,故沉淀质量为4.6g+0.23mol×17g/mol=8.51g,
故选B.
| 4.48L |
| 22.4L/mol |
| 0.336L |
| 22.4L/mol |
最终生成沉淀为Cu(OH)2和Mg(OH)2,根据电荷守恒可知,金属失去电子物质的量等于沉淀中氢氧根的物质的量,故沉淀质量为4.6g+0.23mol×17g/mol=8.51g,
故选B.
点评:本题考查混合物计算,侧重解题方法与分析思维能力的考查,注意利用守恒法解答,难度中等.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
下列仪器使用前必须检查其是否漏水的是( )
①分液漏斗 ②蒸馏烧瓶 ③冷凝管 ④容量瓶 ⑤蒸发皿 ⑥长颈漏斗.
①分液漏斗 ②蒸馏烧瓶 ③冷凝管 ④容量瓶 ⑤蒸发皿 ⑥长颈漏斗.
| A、②⑥ | B、①④ | C、③④ | D、③⑤ |
下列气体中,不能用排空气收集的是( )
| A、NO |
| B、NO2 |
| C、CO2 |
| D、H2 |
化学与人类生活、能源开发、资源利用等密切相关.下列说法正确的是( )
| A、塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用 |
| B、“绿色化学”的核心是利用化学原理,解决和治理环境污染问题 |
| C、硅燃烧放出的热量多,且燃烧产物对环境污染程度低,可做“未来石油” |
| D、秸秆的综合利用,如发酵制沼气、生产乙醇等,工艺复杂,还不如一把火烧光还田来得方便 |
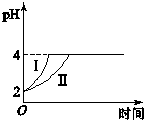 在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )
在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )| A、曲线Ⅰ表示盐酸的pH变化 |
| B、曲线Ⅱ表示盐酸的pH变化 |
| C、在相同条件下,两溶液生成的气体体积相等 |
| D、醋酸溶液中加入锌的质量比盐酸溶液中多 |
表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg
,则下列叙述正确的是( )
| c(H+) |
| c(OH) |
| A、中性溶液的AG=0 |
| B、常温下0.lmol/L氢氧化钠溶液AG=12 |
| C、酸性溶液的AG<0 |
| D、常温下0.lmol/L盐酸溶液的AG=12 |
下列有关说法正确的是( )
| A、铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 |
| B、用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
| C、一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H>0 |
| D、SO2(g)+2CO(g)?2CO2(g)+S(l)达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高 |