题目内容
13.下列物质名称书写正确的是( )| A. | 石炭酸 | B. | 甘胺酸 | C. | 异二戊烯 | D. | 硬酯酸钠 |
分析 A.苯酚俗名为石炭酸;
B.氨基乙酸为甘氨酸;
C.主链含5个C,含2个双键;
D.油脂在碱性条件下水解可生成硬脂肪酸钠.
解答 解:A.苯酚俗名为石炭酸,名称合理,故A正确;
B.氨基乙酸为甘氨酸,胺应为氨,故B错误;
C.主链含5个C,含2个双键,名称应为异戊二烯,故C错误;
D.油脂在碱性条件下水解可生成硬脂肪酸钠,酯应为脂,故D错误;
故选A.
点评 本题考查酸、盐及有机物的名称,为高频考点,把握物质的组成、俗名、有机物的结构与性质为解答的关键,侧重分析与应用能力的考查,注意结合性质分析名称,题目难度不大.

练习册系列答案
相关题目
3.下列物质的使用,不涉及化学变化的是( )
| A. | 氢氟酸刻蚀玻璃 | B. | 生石灰做干燥剂 | ||
| C. | 液氨做制冷剂 | D. | 氢氧化铝可作胃酸中和剂 |
4.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| B. | pH=12的溶液中:K+、NO3-、I-、Na+、AlO2- | |
| C. | Na2S溶液中:K+、SO42-、Cl-、Cu2+ | |
| D. | 由水电离的c(H+)=1.0×10-13 mol/L的溶液中:C6H5O-、K+、SO42-、C1- |
1.室温时,等体积、浓度均为0.1mol/L的下列水溶液,分别达到平衡.
①醋酸溶液:CH3COOH?CH3COO+H+
②醋酸钠溶液:CH3COO-+H2O?CH3COOH+OH-.
有关叙述中正确的是( )
①醋酸溶液:CH3COOH?CH3COO+H+
②醋酸钠溶液:CH3COO-+H2O?CH3COOH+OH-.
有关叙述中正确的是( )
| A. | 加入等体积水后,只有②中平衡向右移动 | |
| B. | 加入等体积水后,①中c(OH-)增大,②中c(OH-)减小 | |
| C. | ①和②中,由水电离出的c(H+)相等 | |
| D. | c(CH3COOH)与c(CH3COO-)之和:①>② |
8.下列化学用语书写正确的是( )
| A. | NH3分子的结构式: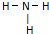 | B. | CO2分子模型的示意图: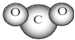 | ||
| C. | 氮分子的结构式:N=N | D. | HClO的电子式: |
18.以氮化镓(GaN)、碳化硅、金刚石等为代表的第三代半导体材料具有高发光效率、抗腐蚀、化学稳定性好、高强度等特性,是目前最先进的半导体材料.
完成下列填空:
(1)组成上述三种半导体材料的各种元素中,原子半径最小的元素在周期表中的位置是第二周期第ⅤA主族.原子序数最小的元素原子的核外电子排布式是1s22s22p2.
(2)镓元素的相对原子质量为69.72,自然界中的镓共有两种稳定的同位素,其中69Ga的原子个数百分含量为60.1%,则另一种镓的同位素可表示为3171Ga.
(3)镓、铝为同族元素,性质相似.下表是两种两性氢氧化物的电离常数.
①写出氢氧化镓的电离方程式:H++H2O+GaO2-?Ga(OH)3?Ga3++3OH-.
②将一块镓铝合金完全溶于烧碱溶液,再往反应后的溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(4)碳化硅单晶是目前技术最成熟的第三代半导体材料.下列能说明碳的非金属性强于硅的反应(或反应组)是ac(选填编号)
a.SiO32-+2CO2+2H2O→H2SiO3+2HCO3-
b.SiO2+2C$\stackrel{高温}{→}$Si+2CO↑
c.SiH4$\stackrel{500℃}{→}$Si+2H2;CH4$\stackrel{>1000℃}{→}$C+2H2
d.Si+O2$\stackrel{900℃}{→}$SiO2;C+O2$\stackrel{300℃}{→}$CO2.
完成下列填空:
(1)组成上述三种半导体材料的各种元素中,原子半径最小的元素在周期表中的位置是第二周期第ⅤA主族.原子序数最小的元素原子的核外电子排布式是1s22s22p2.
(2)镓元素的相对原子质量为69.72,自然界中的镓共有两种稳定的同位素,其中69Ga的原子个数百分含量为60.1%,则另一种镓的同位素可表示为3171Ga.
(3)镓、铝为同族元素,性质相似.下表是两种两性氢氧化物的电离常数.
| 两性氢氧化物 | Al(OH)3 | Ga(OH)3 |
| 酸式电离常数Kia | 2×10-11 | 1×10-7 |
| 碱式电离常数Kib | 1.3×10-33 | 1.4×10-34 |
②将一块镓铝合金完全溶于烧碱溶液,再往反应后的溶液中缓缓通入CO2,最先析出的氢氧化物是Al(OH)3.
(4)碳化硅单晶是目前技术最成熟的第三代半导体材料.下列能说明碳的非金属性强于硅的反应(或反应组)是ac(选填编号)
a.SiO32-+2CO2+2H2O→H2SiO3+2HCO3-
b.SiO2+2C$\stackrel{高温}{→}$Si+2CO↑
c.SiH4$\stackrel{500℃}{→}$Si+2H2;CH4$\stackrel{>1000℃}{→}$C+2H2
d.Si+O2$\stackrel{900℃}{→}$SiO2;C+O2$\stackrel{300℃}{→}$CO2.
5.下列物质的熔点,前者大于后者的是( )
| A. | 晶体硅、碳化硅 | B. | 甲苯、苯酚 | C. | 氧化镁、氧化钠 | D. | 钾钠合金、钠 |
2.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 垃圾是放错地方的资源,应分类回收利用 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 为提高农作物的产量和质量,应大量使用化肥和农药 |
3.分析表提供的数据,下列说法正确的是( )
| 化学式 | 电离常数 |
| HClO | Ki=3×10-8 |
| H2CO3 | Ki1=4.3×10-7 |
| Ki2=5.6×10-11 |
| A. | 84消毒液(有效成分为NaClO)能杀菌的原因:2ClO-+H2O+CO2→2HClO+CO32- | |
| B. | 25°C时,0.1 mol/L NaClO的pH大于0.1 mol/LNaHCO3的pH | |
| C. | 25°C时,0.1 mol/L NaClO的pH大于0.1 mol/L Na2CO3的pH | |
| D. | 0.1 mol/L NaClO和0.1 mol/L NaHCO3溶液中:c(ClO-)>c(HCO3-) |