题目内容
7.下列图示实验装置正确的是( )| A. |  制乙烯 | B. |  测量SO2的体积 | C. |  铁丝燃烧 | D. |  喷泉实验 |
分析 A.实验室用乙醇和浓硫酸制取乙烯时,温度计测量混合溶液温度;
B.二氧化硫和水反应生成亚硫酸;
C.铁丝在氧气中剧烈燃烧,在集气瓶底部应该加入少量水或沙子;
D.饱和食盐水抑制氯气溶解.
解答 解:A.实验室用乙醇和浓硫酸制取乙烯时,温度计测量混合溶液温度,需要170℃,温度计水银球不位于溶液中,故A错误;
B.二氧化硫和水反应生成亚硫酸,苯能隔绝二氧化硫和水反应,所以可以测量收集气体体积,故B正确;
C.铁丝在氧气中剧烈燃烧,在集气瓶底部应该加入少量水或沙子,否则易炸裂集气瓶,故C错误;
D.饱和食盐水抑制氯气溶解,所以不能产生大的压强差,则不能产生喷泉实验,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器的使用、气体收集、基本操作等知识点,明确实验原理及基本操作规范性是解本题关键,注意形成喷泉实验的条件,易错选项是B.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列有关实验原理或操作正确的是( )

| A. | ①液体分层,下层呈无色 | |
| B. | ②洗涤沉淀时,向漏斗中加适量水,搅拌并滤干 | |
| C. | ③分离CCl4和水 | |
| D. | ④除去氯气中的氯化氢 |
15.能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一.
(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图:

则CO2与H2反应生成CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH;
I.CH4(g)+H2O(g)?CO(g)+3H2(g)△H1>0
II.CO(g)+2H2(g)?CH3OH(g)△H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图所示.

①已知温度为T1℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.003 mol•L-1•min-1;
②图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1;.
③若反应II在恒容密闭容器进行,下列能判断反应II达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
④在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
若5min时只改变了某一条件,10min时测得各物质浓度如表,则所改变的条件是向容器中充入1molH2;10min时v正>v逆(填“<”、“>”或“=”).
(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图:

则CO2与H2反应生成CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH;
I.CH4(g)+H2O(g)?CO(g)+3H2(g)△H1>0
II.CO(g)+2H2(g)?CH3OH(g)△H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图所示.

①已知温度为T1℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为0.003 mol•L-1•min-1;
②图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1;.
③若反应II在恒容密闭容器进行,下列能判断反应II达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
④在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
12.表为部分短周期元素化合价及相应氢化物沸点的数据:
已知:
①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙.
请回答:
(1)表中属于第二周期元素的是H、D、B、F(用元素符号填写).
(2)写出G的最高价氧化物的水化物的化学式:HClO4.
(3)比较A、D、F三种元素简单阴离子的半径大小:rS2->rF->rO2-(均用离子符号表示).
(4)AD2与 BD2混合即发生反应,该反应的化学方程式为:SO2+NO2=SO3+NO.
(5)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:SOCl2+H2O=SO2↑+2HCl.
(6)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3═2X+CO2,X的化学式应为NaNO2.
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
| 最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
| 最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
①A与D可形成化合物AD2、AD3,可用于制备强酸甲;
②B与D可形成化合物BD、BD2,可用于制备强酸乙.
请回答:
(1)表中属于第二周期元素的是H、D、B、F(用元素符号填写).
(2)写出G的最高价氧化物的水化物的化学式:HClO4.
(3)比较A、D、F三种元素简单阴离子的半径大小:rS2->rF->rO2-(均用离子符号表示).
(4)AD2与 BD2混合即发生反应,该反应的化学方程式为:SO2+NO2=SO3+NO.
(5)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:SOCl2+H2O=SO2↑+2HCl.
(6)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3═2X+CO2,X的化学式应为NaNO2.
16.下列说法不正确的是( )
| A. | ⅠA族元素的金属性一定比ⅡA族元素的金属性强 | |
| B. | ⅥA族元素中氢化物最稳定的其沸点一定最高 | |
| C. | 非金属元素形成的化合物中也可能是离子化合物 | |
| D. | 离子化合物中可能含有共价键 |
17.对下列事实的解释正确的是( )
| A. | 二氧化硫气体能用浓硫酸干燥,是因为二氧化硫无还原性 | |
| B. | 医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡不溶于盐酸 | |
| C. | 向50 mL 18 mol•L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45 mol | |
| D. | 常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓H2SO4不反应 |
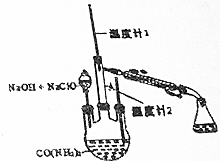 水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应:
水合肼(N2H4•H2O)常用作还原剂和抗氧剂,其熔点为-40℃,沸点118.5℃,极毒.实验室用如下装置制取水合肼(N2H4•H20)涉及下列反应: