题目内容
4.某小组探究金属铜与一定物质的量浓度的HNO3反应,将制得的气体通过浓硫酸后被完全吸收,由此做出猜想:①NO2溶于浓硫酸或与浓硫酸反应;②NO溶于浓硫酸或与浓硫酸反应,并进行下列实验:实验一:将制得的纯净的NO2通入浓硫酸中,溶液变成棕黄色,加热浓硫酸,气体逸出,溶液颜色褪去;
实验二:将制得的纯净的NO通过浓硫酸后用排水集气法收集到足量无色气体,通入氧气后气体变成红棕色;
(1)由此得出的结论是NO2溶于浓硫酸但不与浓硫酸反应,NO不溶于浓硫酸也不与浓硫酸反应.
(2)查阅资料得知:NO、NO2等体积通入浓硫酸中反应生成NOHSO4(其中氮化合价为+3价),气体被全部吸收,试写出此反应的化学方程式NO+NO2+2H2SO4=2NOHSO4+H2O.
(3)为制得干燥的NO2,可将湿润的NO2通过无水氯化钙干燥.也可用Pb(NO3)2加热制得含有NO2的混合气体,并用冰盐水冷却后可得到纯净的液态NO2,已知Pb(NO3)2受热分解的产物中有PbO,试写出加热Pb(NO3)2反应的方程式2Pb(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2PbO+4NO2↑+O2↑.
分析 (1)由实验一和实验二中的现象分析;
(2)NO、NO2等体积通入浓硫酸中反应生成NOHSO4,根据原子守恒书写方程式;
(3)NO2能溶于浓硫酸,NO2与无水氯化钙不反应;Pb(NO3)2加热分解生成NO2和PbO、O2.
解答 解:(1)实验一:将制得的纯净的NO2通入浓硫酸中,溶液变成棕黄色,加热浓硫酸,气体逸出,溶液颜色褪去,说明NO2溶于浓硫酸但不与浓硫酸反应;
实验二:将制得的纯净的NO通过浓硫酸后用排水集气法收集到足量无色气体,通入氧气后气体变成红棕色,说明NO不溶于浓硫酸也不与浓硫酸反应;
故答案为:NO2溶于浓硫酸但不与浓硫酸反应,NO不溶于浓硫酸也不与浓硫酸反应;
(2)NO、NO2等体积通入浓硫酸中反应生成NOHSO4,由原子守恒书写出方程式为NO+NO2+2H2SO4=2NOHSO4+H2O;
故答案为:NO+NO2+2H2SO4=2NOHSO4+H2O;
(3)能溶于浓硫酸,所以不能用浓硫酸干燥NO2,NO2与无水氯化钙不反应,所以可以用无水氯化钙干燥NO2;Pb(NO3)2加热分解生成NO2和PbO、O2,反应方程式为:2Pb(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2PbO+4NO2↑+O2↑;
故答案为:无水氯化钙;2Pb(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2PbO+4NO2↑+O2↑.
点评 本题考查了氮的氧化物的性质、干燥剂的选择、化学方程式等,题目难度中等,侧重于考查学生的分析能力和对题中信息的应用能力.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
9.碳碳双键不能自由转动,所以R-CH=CH-R′(R、R′为烃基)可有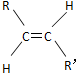 和
和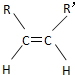 两种空间形式(同分异构体),判断下列化合物中具有上述两种空间排列形式的是( )
两种空间形式(同分异构体),判断下列化合物中具有上述两种空间排列形式的是( )
 和
和 两种空间形式(同分异构体),判断下列化合物中具有上述两种空间排列形式的是( )
两种空间形式(同分异构体),判断下列化合物中具有上述两种空间排列形式的是( )| A. | 乙烯 | B. | 2-戊烯 | C. | 苯乙烯 | D. | 乙烷 |
10.下列实验或叙述不符合绿色化学理念的是( )
| A. | 研制乙醇汽油代替汽油作汽车燃料 | |
| B. | 利用乙烯和氯化氢在催化剂存在的条件下生成氯乙烷 | |
| C. | 在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水 | |
| D. | 用铜和浓H2SO4反应制取Cu SO4 |
7.短周期元素X、Y、Z、W 的原子序数依次增大,X原子的最外层电子数是内层电子数的2倍,X与Z同主族,Y和氢元素同主族,W原子的最外层电子数比次外层电子数少1.下列说法正确的是( )
| A. | 元素X形成的单质一定是原子晶体 | |
| B. | X与Z形成的化合物具有熔点高、硬度大的特点 | |
| C. | Y与氧元素形成的化合物Y2O2中阴、阳离子的个数比为1:1 | |
| D. | W分别与Y、Z形成的化合物中含有的化学键类型相同 |
14.下列关于热化学反应方程式的描述中正确的是( )
| A. | 稀H2SO4和稀Ba(OH)2溶液反应的热化学方程式为:$\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)=$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3kJ/mol | |
| B. | 1molCO(g)完全燃烧时放热283.0kJ,则2CO2(g)=2CO(g)+O2(g)反应的△H=+566kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | NaOH溶液与稀H2SO4反应中和热的化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.6kJ/mol |
13.下列叙述中,正确的是( )
| A. | H2SO4的摩尔质量是98 | |
| B. | 等物质的量的O2和O3中所含的氧原子数相同 | |
| C. | 等质量的CO与CO2中所含碳原子数之比为11:7 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
14.下列化学用语表达正确的是( )
| A. | Cl-离子的结构示意图: | |
| B. | 水分子的电子式: | |
| C. | 乙醇的结构简式:C2H6O | |
| D. | 硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
 醋酸亚铬水合物{[Cr(CH3COO2)]2•2H2O,深红色晶体}易被氧气氧化,是一种氧气吸收剂,通常以二聚体分子的形式存在,不溶于水,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示.
醋酸亚铬水合物{[Cr(CH3COO2)]2•2H2O,深红色晶体}易被氧气氧化,是一种氧气吸收剂,通常以二聚体分子的形式存在,不溶于水,易溶于盐酸.实验室制备醋酸亚铬水合物的装置如图所示.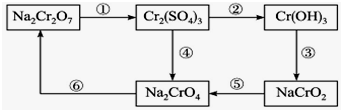 铬是水体的主要的污染物之一,可以导致水生生物死亡.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质.例如处理铬的实验循环示意图如图:
铬是水体的主要的污染物之一,可以导致水生生物死亡.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该有害物质.例如处理铬的实验循环示意图如图: