题目内容
7.锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: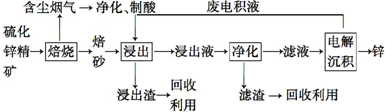
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为ZnO.
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的浸出操作.
(3)浸出液“净化”过程中加入的主要物质为锌粉,其作用是置换出Fe等.
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb-Ag合金惰性电极,阳极逸出的气是O2.
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生主要反应的离子方程式为2ZnS+4H++O2=2Zn2++2S↓+2H2O.
(6)我国古代曾采用“火法”工艺冶炼锌,明代宋应星著的《天工开物》中有关于“升炼倭铅”的记载:“炉甘石十斤,装载入一泥罐内,…,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…,冷淀,毁罐取出,…,即倭铅也.”该炼锌工艺过程主要反应的化学方程式为ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑.(注:炉甘石的主要成分为碳酸锌,倭铅是指金属锌)
分析 硫化锌精矿的焙烧可生成ZnO、氧化铁等,含尘烟气含有含硫氧化物,可用于制备硫酸,浸出液加入硫酸可生成硫酸锌、硫酸铁,加入过量锌充分反应,可置换出铁,滤液中主要含有硫酸锌,经电解可得到锌和硫酸,电解液中含有硫酸,可循环利用,
(1)硫化锌精矿主要成分是ZnS,ZnS在氧气燃烧发生氧化还原反应,据此判断锌的存在形式;
(2)ZnS在氧气燃烧发生氧化还原反应生成产物出来氧化锌外还有硫的氧化物,可转换为硫酸,用于后续的浸出操作;
(3)锌的活泼性强于铁,能够与二价铁离子反应生成铁;
(4)电解沉积过程中,是电解ZnSO4,阳极发生氧化反应,据此判断产物;
(5)依据题意“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质,可知反应物中含有H+和O2,可以获得非金属单质S,据此写出方程式;
(6)由题意可知:反应物为ZnCO3和C,产物含有Zn,根据反应物和生成物写出化学方程式.
解答 解:硫化锌精矿的焙烧可生成ZnO、氧化铁等,含尘烟气含有含硫氧化物,可用于制备硫酸,浸出液加入硫酸可生成硫酸锌、硫酸铁,加入过量锌充分反应,可置换出铁,滤液中主要含有硫酸锌,经电解可得到锌和硫酸,电解液中含有硫酸,可循环利用,
(1)ZnS在氧气燃烧发生氧化还原反应,所以产生焙砂的主要成分的化学式为ZnO,故答案为:ZnO;
(2)ZnS在氧气燃烧发生氧化还原反应生成产物出来氧化锌外还有硫的氧化物,可转换为硫酸,用于后续的浸出操作,
故答案为:浸出;
(3)该含锌矿中还含有FeS等杂质,浸出操作后转化为亚铁离子,可加入锌粉出去亚铁离子,离子方程式:Zn+Fe2+=Zn2++Fe,
故答案为:锌粉;置换出Fe等;
(4)电解沉积过程中,是电解ZnSO4,阳极发生氧化反应,氢氧根离子在阳极上失去电子发生氧化反应生成氧气,
故答案为:O2;
(5)“氧压酸浸”法顾名思义,可知反应物中含有H+和O2,可以获得非金属单质S,化学方程式为:2ZnS+4H++O2=2Zn2++2S↓+2H2O,
故答案为:2ZnS+4H++O2=2Zn2++2S↓+2H2O;
(6)由题意可知:反应物为ZnCO3和C,产物含有Zn,化学方程式:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑,
故答案为:ZnCO3+2C$\frac{\underline{\;高温\;}}{\;}$Zn+3CO↑.
点评 本题为工艺流程题,通过锌的炼制考查了化学方程式、离子方程式的书写,明确工艺流程及各种物质的性质是解题关键,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | NH4Cl固体 | B. | H2SO4 | C. | NaOH固体 | D. | 大量水 |
| A. | X有两种常见氧化物,所含的化学键类型完全相同 | |
| B. | N与M形成的化合物的水溶液显酸性 | |
| C. | 离子半径:N>X,Y>M | |
| D. | 气态氢化物的稳定性:Y>M |
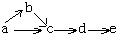 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
| A. | N2 | B. | C12 | C. | Si | D. | C |
| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
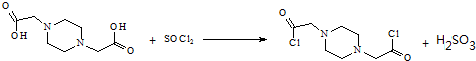 .
.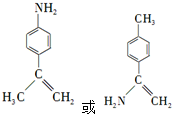 .
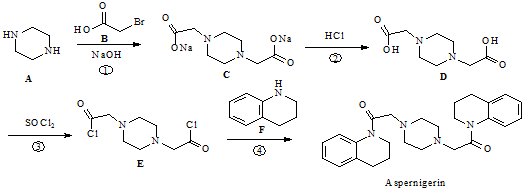
.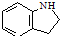 为原料,利用上述有关信息,写出制备
为原料,利用上述有关信息,写出制备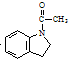 的合成路线流程图(无机试剂任用).合成路线流程图例如下:CH2═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH
的合成路线流程图(无机试剂任用).合成路线流程图例如下:CH2═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH .
.