题目内容
下列各组离子在溶液中一定能够大量共存的是( )
| A、在含有大量OH-的溶液中:NO3-、Na+、Cl-、AlO2- |
| B、在强酸性溶液中:K+、HCO3-、SO42- |
| C、在含有大量SO42-的溶液中:Mg2+、Na+、Cu2+、Cl- |
| D、在含有大量Fe2+的溶液中:H+、Na+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.NO3-、Na+、Cl-、AlO2-离子之间不满足离子反应发生条件,也不与氢氧根离子反应;
B.强酸性溶液中存在大量的氢离子,碳酸氢根离子与氢离子反应生成二氧化碳气体;
C.Mg2+、Na+、Cu2+、Cl-离子之间不发生反应,也不与硫酸根离子反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
B.强酸性溶液中存在大量的氢离子,碳酸氢根离子与氢离子反应生成二氧化碳气体;
C.Mg2+、Na+、Cu2+、Cl-离子之间不发生反应,也不与硫酸根离子反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
解答:
解:A.NO3-、Na+、Cl-、AlO2-之间不发生反应,也不与氢氧根离子反应,在溶液中能够大量共存,故A正确;
B.HCO3-与强酸中的氢离子反应生成二氧化碳,在溶液中不能大量共存,故B错误;
C.Mg2+、Na+、Cu2+、Cl-离子之间不满足离子反应发生条件,且都不与硫酸根离子反应,在溶液中能够大量共存,故C正确;
D.NO3-在酸性条件下能够氧化Fe2+离子,在溶液中不能大量共存,故D错误;
故选C.
B.HCO3-与强酸中的氢离子反应生成二氧化碳,在溶液中不能大量共存,故B错误;
C.Mg2+、Na+、Cu2+、Cl-离子之间不满足离子反应发生条件,且都不与硫酸根离子反应,在溶液中能够大量共存,故C正确;
D.NO3-在酸性条件下能够氧化Fe2+离子,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的正误判断,该题是高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能生成难溶物的离子之间;能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
古语道:“人要实,火要虚”.此话的意思是说:做人必须脚踏实地,事业才能有成;燃烧固体燃料需要架空,燃烧才能更旺.从燃烧的条件看,“火要虚”的实质是( )
| A、增大可燃物的热值 |
| B、提高空气中氧气的含量 |
| C、提高可燃物的着火点 |
| D、增大可燃物与空气的接触面积 |
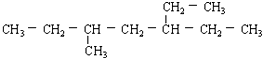 含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )
含有一个双键的烯烃,氢化后的产物结构简式为此烃可能有的结构有( )| A、4种 | B、5种 | C、6种 | D、7种 |
在pH=1的某无色溶液中,下列离子能大量共存的是( )
| A、NH4+、Fe3+、NO3-、CO32- |
| B、Ba2+、NH4+、SO42-、MnO4- |
| C、Na+、Al3+、Cl-、NO3- |
| D、K+、Fe2+、NO3-、SO42- |
0.1mol?L-1 Ba(OH)2溶液与0.1mol?L-1的铵明矾[NH4Al(SO4)2]溶液等体积混合,反应后混合液各离子浓度大小比较合理的是( )
| A、c(SO42-)>c(NH4+)>c(Al3+)>c(OH-)>c(H+) |
| B、c(SO42-)>c(NH4+)>c(Al3+)>c(H+)>c(OH-) |
| C、c(NH4+)>c(SO42-)>c(Al3+)>c(OH-)>c(H+) |
| D、c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-) |
下列关于钠的叙述中,不正确的是( )
| A、钠燃烧时发出黄色的火焰 |
| B、钠燃烧时生成氧化钠 |
| C、实验室少量钠需保存在煤油中 |
| D、钠原子的最外层只有一个电子 |
实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是( )
A、 检查装置气密性 检查装置气密性 |
B、 加热溶液 加热溶液 |
C、 铁丝在氧气中燃烧 铁丝在氧气中燃烧 |
D、 称量 称量 |
