题目内容
10.某化学反应2A?B+D在四种不同条件下进行.B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如表:| 实验序号 | 温度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 820℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 820℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,反应在10至20min时间内平均速率为0.013mol•(L•min)-1.
(2)在实验2中,A的初始浓度c2=1.0mol/L,反应经20min就到达平衡,可推测实验2中还隐含的条件是加入催化剂.
分析 (1)根据平均化学反应速率公式v=$\frac{△c}{△t}$计算;
(2)根据实验1、2数据利用影响速率的因素来分析;
解答 解:(1)v=$\frac{△c}{△t}$=$\frac{(0.8-0.67)mol/L}{10min}$=0.013mol/(L.min),故答案为 0.013;
(2)根据实验1、2数据分析,温度相同,达平衡后A的物质的量浓度相同,且B、D起始浓度为0,所以两组实验中A的起始浓度相同为1.0mol•L-1 ;温度相同,达平衡后A的物质的量浓度相同,但达平衡时2组的时间较短,所以只能是加入催化剂;故答案为:1.0;加入催化剂.
点评 本题考查了化学平衡的分析判断,化学反应速率的计算应用,注意影响平衡因素的分析判断条件,题目难度中等.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
20.下列物质中不能使高锰酸钾酸性溶液褪色的是( )
| A. | 丙烯 | B. | 苯 | C. | 甲苯 | D. | 乙炔 |
18.下列有机物属于芳香族化合物的是( )
| A. | 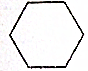 | B. |  | ||
| C. |  | D. |  |
4.化学与生产和生活密切相关,下列说法正确的是( )
| A. | 聚乙烯塑料的老化是因为发生了加成反应 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁能源 | |
| C. | 利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化的过程 | |
| D. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 |
11.苯不能使少量酸性高锰酸钾溶液褪色,但苯的同系物能使少量酸性高锰酸钾溶液褪色,下列解释正确的是( )
| A. | 苯的同系物中原子数比苯分子中原子数多 | |
| B. | 苯环受侧链的影响而易被KMnO4氧化 | |
| C. | 侧链受苯环的影响而易被KMnO4氧化 | |
| D. | 苯环和侧链相互影响,同时被氧化 |
8.下列措施能使铁与稀硫酸反应产生氢气的速率加快的是( )
| A. | 加入Na2SO4溶液 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 滴加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |
9.有关淀粉的叙述中正确的是( )
| A. | 淀粉的分子式是C12H22O11 | |
| B. | 淀粉可以发生银镜反应 | |
| C. | 淀粉可以直接检验食盐中是否含有碘元素 | |
| D. | 淀粉是天然高分子化合物 |
