题目内容
氨与铵盐是一种重要的化工原料.
(1)实验室用NH4Cl制备氨气的化学方程式为 .
(2)制备氨气可用多种方法,实验室制取少量干燥的氨气涉及下列装置,其中正确的是 .

A.①是氨气发生装置 B.③是氨气发生装置 C.②是氨气吸收装置 D.④是氨气收集、检验装置
(3)检验铵盐的方法是 ,发生反应的离子方程式为: .
(1)实验室用NH4Cl制备氨气的化学方程式为
(2)制备氨气可用多种方法,实验室制取少量干燥的氨气涉及下列装置,其中正确的是

A.①是氨气发生装置 B.③是氨气发生装置 C.②是氨气吸收装置 D.④是氨气收集、检验装置
(3)检验铵盐的方法是
考点:氨的实验室制法
专题:
分析:(1)固体氯化铵与氢氧化钙在加热条件下反应生成氨气;
(2)①NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl;
②氨气极易溶于水,装置中相当于导气管直接插入水,容易发生倒吸;
③CaO遇水生成Ca(OH)2,同时放出大量热量,有利于氨气的生成;
④氨气易溶于水,装置图中收集氨气易与空气对流收集不到纯净的气体;
(3)检验铵盐溶液的方法是:利用铵盐和氢氧化钠在加热条件下生成氨气,用湿润红色石蕊试纸来检验,湿润红色石蕊试纸会变蓝色,由原子守恒来判断溶液为铵盐溶液.
(2)①NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl;
②氨气极易溶于水,装置中相当于导气管直接插入水,容易发生倒吸;
③CaO遇水生成Ca(OH)2,同时放出大量热量,有利于氨气的生成;
④氨气易溶于水,装置图中收集氨气易与空气对流收集不到纯净的气体;
(3)检验铵盐溶液的方法是:利用铵盐和氢氧化钠在加热条件下生成氨气,用湿润红色石蕊试纸来检验,湿润红色石蕊试纸会变蓝色,由原子守恒来判断溶液为铵盐溶液.
解答:
解:(1)固体氯化铵与氢氧化钙在加热条件下反应生成氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)A.NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl,气体进入干燥管的机会不多,故①错误;
B.向CaO中滴加浓氨水,CaO遇水生成Ca(OH)2,同时放出大量热量,使浓氨水中的氨气逸出,故③正确;
C.氨气极易溶于水按照装置图水会发生倒吸,故②错误;
D.装置中试管口处应塞一团棉花,氨气易溶于水防止与空气对流,得不到纯净的氨气,故④错误;
故选:B;
(3)检验铵盐溶液的方法是:加热氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验,发生的反应为:NH4++OH-
NH3↑+H2O;
故答案为:加热氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验;NH4++OH-
NH3↑+H2O.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)A.NH4Cl固体受热分解生成NH3和HCl,而当温度降低时,NH3和HCl又重新化合成固体NH4Cl,气体进入干燥管的机会不多,故①错误;
B.向CaO中滴加浓氨水,CaO遇水生成Ca(OH)2,同时放出大量热量,使浓氨水中的氨气逸出,故③正确;
C.氨气极易溶于水按照装置图水会发生倒吸,故②错误;
D.装置中试管口处应塞一团棉花,氨气易溶于水防止与空气对流,得不到纯净的氨气,故④错误;
故选:B;
(3)检验铵盐溶液的方法是:加热氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验,发生的反应为:NH4++OH-
| ||
故答案为:加热氢氧化钠溶液,加热,用湿润的红色石蕊试纸放在试管口检验;NH4++OH-
| ||
点评:本题考查了氨气的实验室制备,明确制备原理和氨气的性质是解题关键,注意氨气的检验和尾气吸收,题目难度不大.

练习册系列答案
相关题目
当氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)?Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的( )
| A、MgCl2 |
| B、NaOH |
| C、MgSO4 |
| D、NaHSO4 |
糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质.下列有关说法正确的是( )
| A、糖类物质中只含有C、H、O三种元素 |
| B、蛋白质遇浓硝酸变成紫色 |
| C、油脂在人体中发生水解生成氨基酸 |
| D、糖类、蛋白质都能发生水解反应 |
下列叙述正确的是( )
| A、利用惰性电极电解饱和食盐水的过程中,溶液中水的电离平衡向左移动 |
| B、溴元素和碘元素被称为“海洋元素” |
| C、向AlCl3溶液中加入氨水可制取Al(OH)3 |
| D、Fe分别与氯气和稀盐酸反应可得到同一种氯化物 |
下列四种x的溶液,分别加入盛有100mL2mol.L-1盐酸的烧杯中,并加入水稀释至500mL,此时x和盐酸缓和地进行反应,其中反应速率最大的是( )
| A、20 mL,3mol.L-1 |
| B、20 mL,2mol.L-1 |
| C、10 mL,4mol.L-1 |
| D、10 mL,2mol.L-1 |
铅蓄电池的总反应式为:PbO2+Pb+2H2SO4
2PbSO4+2H2O,据此判断下列叙述正确的是( )
| 充电 |
| 放电 |
| A、放电时,H2SO4 浓度增加 |
| B、放电时,负极的电极反应式为:Pb+SO42--2e-=PbSO4 |
| C、在充电时,电池中每转移1mol电子,理论上生成1mol硫酸 |
| D、在充电时,阴极发生的反应是PbSO4-2e-+2H2O=PbO2+SO2-4+4H+ |
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( )
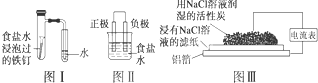

| A、按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B、图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C、铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-═Cl2↑ |
| D、图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成.下列说法不正确的是( )
| A、生产水泥的原料是大理石、纯碱、石英,其组成一般为Na2O?CaO?6SiO2 |
| B、Si与NaOH溶液反应的离子方程式为:Si+2OH-+H2O=SiO32-+2H2↑ |
| C、焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是CO2 |
| D、经处理后的熔渣36.0g(仅含Fe2O3、Al2O3、SiO2),加入足量稀盐酸,分离得到11.0 g固体;滤液中加入过量NaOH溶液,分离得到21.4g固体;则此熔渣中Al2O3的质量分数为25% |
