题目内容
下列四种x的溶液,分别加入盛有100mL2mol.L-1盐酸的烧杯中,并加入水稀释至500mL,此时x和盐酸缓和地进行反应,其中反应速率最大的是( )
| A、20 mL,3mol.L-1 |
| B、20 mL,2mol.L-1 |
| C、10 mL,4mol.L-1 |
| D、10 mL,2mol.L-1 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:先计算出稀释后X溶液的中X的物质的量,最后溶液的体积都为50mL,则物质的量越大,浓度越大,则反应速率越大来判断.
解答:
解:均加水稀释到500mL,
A.n(X)=0.02L×3mol/L=0.06mol;
B.n(X)=0.02L×2mol/L=0.04mol;
C.n(X)=0.01L×4mol/L=0.04mol;
D.n(X)=0.01L×2mol/L=0.02mol,
物质的量最大的是A,则A浓度最大,反应速率最大.
故选A.
A.n(X)=0.02L×3mol/L=0.06mol;
B.n(X)=0.02L×2mol/L=0.04mol;
C.n(X)=0.01L×4mol/L=0.04mol;
D.n(X)=0.01L×2mol/L=0.02mol,
物质的量最大的是A,则A浓度最大,反应速率最大.
故选A.
点评:本题考查反应速率与浓度的关系及物质的量的计算,难度不大,明确影响化学反应速率的因素、物质的量与浓度的关系是解答本题的关键.

练习册系列答案
相关题目
 向Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液时,其沉淀的质量m和所加NaOH体积V之间的关系如图所示,则混合液中Al2(SO4)3与MgSO4的物质的量之比是( )
向Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液时,其沉淀的质量m和所加NaOH体积V之间的关系如图所示,则混合液中Al2(SO4)3与MgSO4的物质的量之比是( )| A、1:1 | B、1:2 |
| C、2:1 | D、1:3 |
 上海世博会上澳大利亚馆的外墙采用的是特 殊的耐风化钢覆层材料,外墙的颜色每天都在发生着变化,它会随空气中太阳、风雨、湿度的影响,逐渐结出一层锈斑,从橙色到赭红色的转变,看上去外观的生锈程度在增加,运用了钢材生锈原理.下列有关钢材生锈的说法正确的是( )
上海世博会上澳大利亚馆的外墙采用的是特 殊的耐风化钢覆层材料,外墙的颜色每天都在发生着变化,它会随空气中太阳、风雨、湿度的影响,逐渐结出一层锈斑,从橙色到赭红色的转变,看上去外观的生锈程度在增加,运用了钢材生锈原理.下列有关钢材生锈的说法正确的是( )| A、红色铁锈的主要成分是Fe(OH)3 |
| B、钢材在空气中的变化只有氧化还原反应 |
| C、空气中太阳、风雨、湿度对钢材的腐蚀有影响 |
| D、钢材在空气中的腐蚀主要为电化学腐蚀,其负极的反应为:Fe-3e-=Fe3+ |
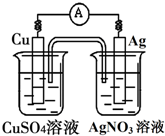 已知反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是( )
已知反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)为一自发进行的氧化还原反应,将其设计成如图所示原电池.下列说法中正确的是( )| A、铜电极是正极,其电极反应为Cu-2e-=Cu2+ |
| B、银电极上发生还原反应,电极质量增加 |
| C、当铜电极质量减少0.64g时,电解质溶液中有0.02mol电子通过 |
| D、外电路中电子由银电极流向铜电极 |
下列说法正确的是( )
| A、分解反应一定是氧化还原反应 |
| B、非金属单质在氧化还原反应中一定作氧化剂 |
| C、氧化剂具有氧化性,还原剂具有还原性 |
| D、氧化剂在氧化还原反应中被氧化 |
已知C4H9Cl的同分异构体数是4种,则C4H10O中属于醇类的同分异构体数目是( )
| A、2 | B、3 | C、4 | D、5 |
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.