��Ŀ����
���³�ѹ��,��a mol CO2����ͨ��1 L b mol/L��NaOH��Һ��,���ж�������Һ����������ȷ���ǣ� ��
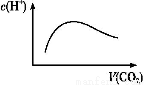
A.��a=2bʱ,����CO2�����ͨ��,��Һ����ˮ�������c(H+)����ͼ�仯��ϵ
B.��a=bʱ,������Һ�д���:c(OH-)+c(C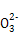 )=c(H+)+c(H2CO3)
)=c(H+)+c(H2CO3)
C.��2a=bʱ,������Һ�д���:c(Na+)��c(C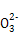 )��c(OH-)��c(HC
)��c(OH-)��c(HC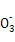 )��c(H+)
)��c(H+)
D.��1/2��a/b��1ʱ,������Һ��һ������:c(Na+)=c(C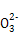 )+c(HC
)+c(HC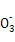 )+c(H2CO3)
)+c(H2CO3)
D
����������a=2bʱ,��CO2��ͨ��CO2��NaOH��Ӧ������Na2CO3,�̶�����NaHCO3,��������CO2��H2CO3��ʽ��������Һ��,�����ε�ˮ��ٽ�ˮ�ĵ���,����������ˮ�ĵ���,A��;��a=bʱ,CO2��NaOH��Ӧ����NaHCO3,���������غ��֪c(OH-)=c(H2CO3)+[c(H+)-c(C )],B��;��2a=bʱ,CO2��NaOH��Ӧ����Na2CO3,c(OH-)��C
)],B��;��2a=bʱ,CO2��NaOH��Ӧ����Na2CO3,c(OH-)��C ˮ���ˮ�ĵ����������ṩ,��c(OH-)��c(HC
ˮ���ˮ�ĵ����������ṩ,��c(OH-)��c(HC ),C��;��1/2��a/b��1ʱ,CO2��NaOH��Ӧ����Na2CO3��NaHCO3,���������غ�,c(Na+)��c(C
),C��;��1/2��a/b��1ʱ,CO2��NaOH��Ӧ����Na2CO3��NaHCO3,���������غ�,c(Na+)��c(C )+c(HC
)+c(HC )+c(H2CO3)��
)+c(H2CO3)�� c(Na+),D����
c(Na+),D����

 ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д�
ѧ�����νӽ̲��Ͼ���ѧ������ϵ�д� Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
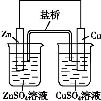
��ʿһ��ȫͨϵ�д����ӹ�ҵ����30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ��,����ӡˢ��·�塣ij����ʦΪ�˴ӷ�Һ�л���ͭ,���»��FeCl3��Һ,���������ʵ�鲽��:

д��һ����֤����ԭ��Fe��Cuǿ�����ӷ���ʽ: ��
�÷�Ӧ����ͼ���� �з����������������Ӧ���һ��ԭ���,�ڷ����л�������װ��ͼ(����缫���ơ��缫���ϡ��������Һ)��
|
�������̻��յ�ͭ�Ǵ�ͭ,Ϊ�˻�ø�����ͭ������е�⾫����д����⾫��ʱ�������ϼ���Ҫ�ĵ缫��Ӧʽ ��
��֪�ϳɰ���ӦN2(g)+3H2(g) 2NH3(g) ��H=-92.20 kJ��mol-1,��ij�¶���2 L���ܱ������н���,�����������:
2NH3(g) ��H=-92.20 kJ��mol-1,��ij�¶���2 L���ܱ������н���,�����������:
ʱ��(h) ���ʵ���(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | n5 |
H2 | 4.50 | 4.20 | 3.60 | n4 | n6 |
NH3 | 0 | 0.20 | n2 | 1.00 | 1.00 |
����˵����ȷ���ǣ� ��
A.��Ӧ3 h��,��Ӧ����v(N2)Ϊ0.17 mol��L-1��h-1
B.���¶���,�÷�Ӧ��ƽ�ⳣ��Ϊ0.037
C.��Ӧ���е�1 hʱ�ų�������Ϊ9.22 kJ
D.4 hʱ,���ټ���1 mol N2,�ﵽ�µĻ�ѧƽ��ʱ,N2��ת������ԭ��������