题目内容
已除去泥沙的粗盐中,仍含有Mg2+、Ca2+和SO42-,请填写下列空格,完成将粗盐提纯,得到氯化钠晶体的实验设计.
实验目的:粗盐提纯,得到纯净氯化钠晶体
实验用品:粗盐、NaOH溶液、HCl溶液、Na2CO3溶液、BaCl2溶液、pH试纸、蒸馏水 仪器(略)
(1)填写下表中所缺实验步骤和操作过程(a~e):
(2)实验问题讨论:实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯 ②固定铁圈的位置 ③放上蒸发皿 ④加热搅拌 ⑤停止加热、余热蒸干.其正确的操作顺序是 .
A.①②③⑤④B.①②③④⑤C.②③①④⑤D.②①③④⑤
实验目的:粗盐提纯,得到纯净氯化钠晶体
实验用品:粗盐、NaOH溶液、HCl溶液、Na2CO3溶液、BaCl2溶液、pH试纸、蒸馏水 仪器(略)
(1)填写下表中所缺实验步骤和操作过程(a~e):
| 序号 | 实验步骤 | 简述实验操作 (不必叙述如何组装实验装置) |
| ① | 将粗盐放入烧杯中,加入适时的蒸馏水,充分搅拌,直至固体全部消失 | |
| ② | 加入NaOH溶液 | 逐滴加入氢氧化钠溶液,直至不再出现沉淀为止 |
| ③ | 加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
| ④ | 加入 |
逐滴加入该溶液,直至不再出现沉淀为止 |
| ⑤ | 过滤 | 安装好过滤器,将④烧杯中的悬浊液沿玻璃棒加入过滤器中过滤 |
| ⑥ | 滴加盐酸 | 向滤液中逐滴加入盐酸,并用pH试纸检测溶液,至溶液呈中性 |
| ⑦ |
A.①②③⑤④B.①②③④⑤C.②③①④⑤D.②①③④⑤
考点:粗盐提纯
专题:实验题
分析:(1)除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,先加入过量的氢氧化钠溶液除去镁离子,然后加入足量的氯化钡溶液除去硫酸根离子,然后加入过量的碳酸钠溶液除去钙离子和过量的钡离子,最后加入过量的盐酸除去过量的氢氧根离子和碳酸根离子,氯化氢易挥发,加热可以除去过量的氯化氢;
蒸发时应该把溶液放入蒸发皿中加热,待出现较多固体时,停止加热,利用余热使滤液蒸干;
(2)实验仪器的组装一般遵循:由下到上,由左到右的原则,据此解答.
蒸发时应该把溶液放入蒸发皿中加热,待出现较多固体时,停止加热,利用余热使滤液蒸干;
(2)实验仪器的组装一般遵循:由下到上,由左到右的原则,据此解答.
解答:
解:(1)要除去粗盐中的杂质离子,首先将粗盐放入烧杯中,加入适时的蒸馏水,然后加入过量的氢氧化钠溶液直至不再出现沉淀为止,再加入加入足量的氯化钡溶液除去硫酸根离子,然后加入过量的碳酸钠溶液除去钙离子和过量的钡离子,最后加入过量的盐酸除去过量的氢氧根离子和碳酸根离子,氯化氢易挥发,加热可以除去过量的氯化氢,蒸发时注意:把溶液放入蒸发皿中加热,待出现较多固体时,停止加热,利用余热使滤液蒸干;
故答案为:溶解;BaCl2溶液;Na2CO3溶液;蒸发;把溶液放入蒸发皿中加热,待出现较多固体时,停止加热,利用余热使滤液蒸干;
(2)组装仪器时要从下向上,从左到右组装,酒精灯放在铁圈和蒸发皿的下方,所以要先放酒精灯;然后再固定铁圈,放置蒸发皿,然后再点燃酒精灯加热,并搅拌,当有较多晶体析出时,停止加热,借余热蒸干,
故答案为:B.
故答案为:溶解;BaCl2溶液;Na2CO3溶液;蒸发;把溶液放入蒸发皿中加热,待出现较多固体时,停止加热,利用余热使滤液蒸干;
(2)组装仪器时要从下向上,从左到右组装,酒精灯放在铁圈和蒸发皿的下方,所以要先放酒精灯;然后再固定铁圈,放置蒸发皿,然后再点燃酒精灯加热,并搅拌,当有较多晶体析出时,停止加热,借余热蒸干,
故答案为:B.
点评:本题考查了粗盐的提纯、蒸发实验的操作及注意事项,题目难度不大,注意蒸发时待出现较多固体时,停止加热,利用余热使滤液蒸干.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列有关物质性质的叙述正确的是( )
| A、MgO和Fe3O4都能与铝发生铝热反应 |
| B、乙醇和乙酸都能发生取代反应 |
| C、乙烷和苯都不能发生氧化反应 |
| D、NaCl溶液和蛋白质溶液都不能产生丁达尔效应 |
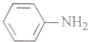 )具有
)具有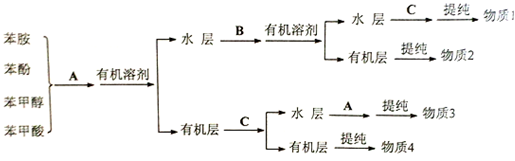
 转化为
转化为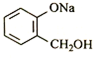 ,则应加入
,则应加入 实验室配制480mL 0.1mol?L-1NaOH溶液,回答下列问题
实验室配制480mL 0.1mol?L-1NaOH溶液,回答下列问题