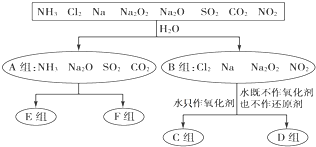
题目内容
乙烯是一种重要的化工原料,下列有关乙烯的说法中正确的是( )
| A、乙烯和苯的分子结构均含有碳碳双键 |
B、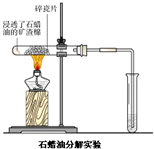 如图石蜡油分解产生的气体只有乙烯,能使溴的CCl4溶液褪色 |
| C、乙烯的产量可以用来衡量一个国家的石油化工生产水平 |
| D、工业常用乙烯与水发生加成反应生产食用酒精 |
考点:乙烯的化学性质
专题:有机物的化学性质及推断
分析:A、乙烯中含有双键,苯中不含有不饱和的双键;
B、石蜡油的分解产物是混合物;
C、乙烯的产量可以用来衡量一个国家的石油化工生产水平;
D、乙烯与水加成得到工业酒精.
B、石蜡油的分解产物是混合物;
C、乙烯的产量可以用来衡量一个国家的石油化工生产水平;
D、乙烯与水加成得到工业酒精.
解答:
解:A、乙烯中含有双键,苯中不含有不饱和的双键,故A错误;
B、石蜡油的分解产物是混合物,含有乙烯,能使高锰酸钾溶液褪色,故B错误;
C、乙烯的产量可以用来衡量一个国家的石油化工生产水平,故C正确;
D、乙烯与水加成得到的酒精为工业酒精,故D错误;
故选C.
B、石蜡油的分解产物是混合物,含有乙烯,能使高锰酸钾溶液褪色,故B错误;
C、乙烯的产量可以用来衡量一个国家的石油化工生产水平,故C正确;
D、乙烯与水加成得到的酒精为工业酒精,故D错误;
故选C.
点评:本题主要考查的是常见有机物的化学性质,涉及石油的分馏、乙烯的加成反应,苯的结构等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应 |
| B、高温或日常用的消毒剂可使禽流感病毒蛋白质变性 |
| C、棉花、羊毛、木材和草类的主要成分都是纤维素 |
| D、误食重金属盐引起人体中毒,可喝大量的食盐水解毒 |
化合物C是制备液晶材料的中间体之一,它可由A和B在一定条件下制得下列说法正确的是( )


| A、每个A分子中含有1个手性碳原子 |
| B、可以用酸性KMnO4溶液检验B中是否含有醛基 |
| C、1molC分子最多可与4molH2发生加成反应 |
| D、C可发生加成反应、取代反应、氧化反应、消去反应 |
 非血红素铁是食物中的铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.
非血红素铁是食物中的铁存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物.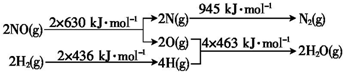 H2还原NO生成氮气和水蒸气的热化学方程式是
H2还原NO生成氮气和水蒸气的热化学方程式是