题目内容
氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.
(1)工业上一般采用CO和H2反应合成可再生能源甲醇.反应如下:CO(g)+2H2(g)?CH3OH(g)△H=-90.1KJ?mol-1在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol?L-1)变化如下表所示:(前6min没有改变条件)
①x= .
②250℃时该反应的平衡常数K的计算式为: (不必化简).
③若6min~8min只改变了某一条件,所改变的具体条件是 .
④第8min时,该反应是不是达到平衡状态 .(填“是”或“不是”)
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2.
已知: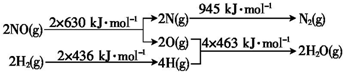 H2还原NO生成氮气和水蒸气的热化学方程式是 .
H2还原NO生成氮气和水蒸气的热化学方程式是 .
(1)工业上一般采用CO和H2反应合成可再生能源甲醇.反应如下:CO(g)+2H2(g)?CH3OH(g)△H=-90.1KJ?mol-1在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol?L-1)变化如下表所示:(前6min没有改变条件)
| 2min | 4min | 6min | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.20 | … |
| CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
②250℃时该反应的平衡常数K的计算式为:
③若6min~8min只改变了某一条件,所改变的具体条件是
④第8min时,该反应是不是达到平衡状态
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2.
已知:
 H2还原NO生成氮气和水蒸气的热化学方程式是
H2还原NO生成氮气和水蒸气的热化学方程式是考点:化学平衡的计算,热化学方程式,化学平衡状态的判断
专题:化学反应中的能量变化,化学平衡专题
分析:(1)①根据表中2min和4min时各种物质的浓度的变化量,依据转化量之比等于方程式计量系数之比可求出x值;
②该反应的平衡常数表达式K=
,将在250℃下,将4min时各物质平衡浓度带入计算;
③根据6min到8min时各物质浓度的变化来确定改变条件;
④求出第8min时反应的浓度商Qc,与250℃时K做比较,若Qc=K反应达到平衡状态;
(2)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量.
②该反应的平衡常数表达式K=
| c(CH3OH) |
| c(CO)?c2(H2) |
③根据6min到8min时各物质浓度的变化来确定改变条件;
④求出第8min时反应的浓度商Qc,与250℃时K做比较,若Qc=K反应达到平衡状态;
(2)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量.
解答:
解:(1)①从图中可知从2min到4min时各物质的转化量为:△C(CO):△C(H2):△C(CH3OH)=(0.07-0.06):(X-0.12):(0.04-0.03)
化学反应中各物质的转化量之比等于方程式的计量系数得:(0.07-0.06):(X-0.12):(0.04-0.03)=1:2:1,解得X=0.14,
故答案为:0.14;
②250℃下,甲醇的平衡浓度是0.06mol/L,氢气的平衡浓度是0.12mol/L,一氧化碳的平衡浓度是0.04mol/L所以平衡常数K=
=
;
故答案为:
;
③对比6min和8min时各物质的浓度可知改变条件后反应反应向正方向进行,按照转化量之比等于计量系数之比△C(CO):△C(H2):△C(CH3OH)=0.01mol/L:0.02mol/L:0.01mol/L,所以8min后三种物质的浓度应为:(0.06-0.01)mol/L、(0.12-0.02)mol/L、(0.04+0.01)mol/L,而8min后氢气的浓度为0.2mol/L,所以多加了0.1mol/L×10=1mol的氢气;
故答案为:加1 mol氢气;
④第8min时反应的浓度商Qc=
=
=
≠K,所以此时不是平衡状态,故答案为:不是;
(2)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ?mol-1,故答案为:2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ?mol-1.
化学反应中各物质的转化量之比等于方程式的计量系数得:(0.07-0.06):(X-0.12):(0.04-0.03)=1:2:1,解得X=0.14,
故答案为:0.14;
②250℃下,甲醇的平衡浓度是0.06mol/L,氢气的平衡浓度是0.12mol/L,一氧化碳的平衡浓度是0.04mol/L所以平衡常数K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.04 |
| 0.06×0.122 |
故答案为:
| 0.04 |
| 0.06×0.122 |
③对比6min和8min时各物质的浓度可知改变条件后反应反应向正方向进行,按照转化量之比等于计量系数之比△C(CO):△C(H2):△C(CH3OH)=0.01mol/L:0.02mol/L:0.01mol/L,所以8min后三种物质的浓度应为:(0.06-0.01)mol/L、(0.12-0.02)mol/L、(0.04+0.01)mol/L,而8min后氢气的浓度为0.2mol/L,所以多加了0.1mol/L×10=1mol的氢气;
故答案为:加1 mol氢气;
④第8min时反应的浓度商Qc=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.05 |
| 0.05×0.22 |
| 1 |
| 0.04 |
(2)根据能量变化图,则反应断键共吸收2×630+2×436=2132kJ,形成共放出945+4×463=2797kJ,所以该反应共放出2797-2132=665kJ的热量,热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ?mol-1,故答案为:2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=-665 kJ?mol-1.
点评:本题考查了化学平衡移动的影响因素、化学平衡常数的计算和应用和盖斯定律求反应热,题目综合性强,涉及知识是高考中常考的内容,难度较大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关环境问题的说法错误的是( )
| A、用天然气代替含硫的煤作燃料,可减少废气中二氧化硫的量 |
| B、臭氧含量过高的空气不利于人体健康 |
| C、溶有大量二氧化碳的降水通常称为酸雨 |
| D、废电池必须回收处理的原因是防止重金属离子污染环境 |
乙烯是一种重要的化工原料,下列有关乙烯的说法中正确的是( )
| A、乙烯和苯的分子结构均含有碳碳双键 |
B、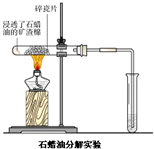 如图石蜡油分解产生的气体只有乙烯,能使溴的CCl4溶液褪色 |
| C、乙烯的产量可以用来衡量一个国家的石油化工生产水平 |
| D、工业常用乙烯与水发生加成反应生产食用酒精 |
在200mL氯化铁和氯化铝的混合液中,Fe3+的物质的量浓度为0.2mol/L,Cl-的物质的量浓度为1.8mol/L.要使Fe3+全部转化为沉淀分离出来,至少需要加入 4mol/L NaOH溶液的体积为( )
| A、30mL | B、110mL |
| C、90mL | D、180mL |
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )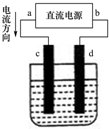

| A、电解过程中,d电极质量增加 |
| B、d为阳极,电极反应为:2Cl--2e-=Cl2↑ |
| C、a为负极、b为正极 |
| D、电解过程中,氯离子浓度不变 |
有关AgCl的沉淀溶解平衡的说法正确的是( )
| A、AgCl难溶于水,溶液中没有Ag+和Cl- |
| B、AgCl沉淀生成和溶解同时在不断进行,且速率相等 |
| C、向AgCl溶液中加入盐酸,一定会有沉淀生成 |
| D、向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化 |
 X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下:
X、Y、Z、M、Q、R是6种短周期元素,其原子半径及主要化合价如下: COOH
COOH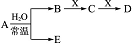 已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).
已知由 C、N、O、Na、Fe五种元素组成的常见单质或化合物存在如图所示转化关系(部分生成物和反应条件略去).