题目内容
14.下列各分子中,所有原子都满足最外层为8电子结构的是( )| A. | H2O | B. | XeF4 | C. | Cl2 | D. | PCl5 |
分析 根据原子最外层电子数和化合价判断,在化合物中,原子最外层电子数等于原子的价层电子数+|化合价|,以此进行分析.
解答 解:A.H2O分子中,氢原子最外层有2个电子,所以氢原子不满足8电子稳定结构,故A错误;
B.XeF4分子中,Xe原子最外层有8个电子,该化合物中Xe形成4个共价键,则Xe原子最外层电子数为:8+4=12,不满足8电子稳定结构,故B错误;
C.Cl2分子中,氯原子最外层有7个电子,两个原子共用1个电子对使两个原子都达到8电子稳定结构,故C正确;
D.PCl5中,P原子的最外层电子为:5+5=10,不满足8电子稳定结构,故D错误;
故选C
点评 本题考查原子核外电子排布,题目难度不大,注意掌握判断是否满足8电子结构的方法,利用化合价与最外层电子数来分析即可解答,明确原子核外电子排布规律及结构特点为解答关键.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
4.下列有机物的命名正确的是( )
| A. | 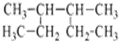 2.3-二乙基丁烷 | B. | 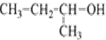 2-丁醇 | C. | 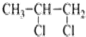 二氯丙烷 | D. | 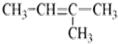 3-甲基-2-丁烯 |
5.对于锌、铜和稀硫酸构成的原电池,下列有关说法正确的是( )
①Zn是负极
②Cu是正极
③负极反应:Zn-2e-=Zn2+
④正极反应:Cu2++2e-=Cu
⑤H+向负极移动
⑥电子由Cu极通过导线向Zn极移动.
①Zn是负极
②Cu是正极
③负极反应:Zn-2e-=Zn2+
④正极反应:Cu2++2e-=Cu
⑤H+向负极移动
⑥电子由Cu极通过导线向Zn极移动.
| A. | 仅①②③⑤ | B. | ①②③④⑤ | C. | 仅②③④⑥ | D. | 仅①②③ |
9.如图为元素周期表短周期中的一部分,有关元素X、Y、Z、M的说法不正确的是( )
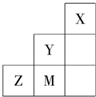

| A. | M、Z可形成ZM2分子 | B. | X原子最外层达到8电子结构 | ||
| C. | 原子半径:Z>M>Y | D. | Z2-的结构示意图可表示为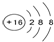 |
19.下列化学用语表示正确的是( )
| A. | 水的电子式: | B. | CH4分子的比例模型: | ||
| C. | 铝的原子结构示意图: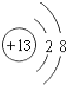 | D. | 乙烯的结构简式:CH2CH2 |
4.下列各种规律描述正确的是( )
| A. | 第ⅠA 族元素单质的熔点随着原子序数递增而升高 | |
| B. | 卤族元素单质的熔点随着原子序数递增而升高 | |
| C. | 第ⅤA族元素的气态氢化物沸点随着原子序数递增而升高 | |
| D. | 第三周期元素形成的简单离子半径随着原子序数递增而增大 |
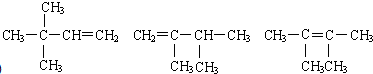 任意一种(写出其中一种即可).
任意一种(写出其中一种即可). ;
;