题目内容
19.下列表示物质的图或式正确的是( )| A. | 氮气的电子式 | B. | Mg2+的结构示意图 | ||
| C. | NH3的结构式  | D. | O22-的电子式为: |
分析 A.氮气分子中,N原子最外层满足8电子稳定结构,该电子式漏掉了N原子的1对未成键电子对;
B.镁离子的核外电子总数为10,最外层含有8个电子;
C.用短线代替所有的共用电子对即为结构式;
D.过氧根离子中两个O原子形成的是O-O单键.
解答 解:A.氮气分子中含有1个氮氮三键,其正确的电子式为 ,故A错误;
,故A错误;
B.Mg2+的质子数为12,电子数为10,离子结构示意图为: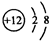 ,故B错误;
,故B错误;
C.氨气分子中含有3个N-H键,NH3的结构式为: ,故C正确;
,故C正确;
D.过氧根中,氧原子之间形成的是非极性共价单键,并且有1对共用电子,正确的电子式为 ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、离子结构示意图、结构式等知识,明确常见化学用语的书写原则为解答关键,试题侧重考查学生的规范答题能力.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
20.已知某原子的结构示意图如图所示,下列说法中错误的是( )


| A. | 该元素位于第三周期第ⅡA族 | B. | 该元素属于非金属元素 | ||
| C. | 该原子有3个电子层 | D. | 该原子最外层有2个电子 |
1.下列离子组能大量共存且溶液无色的是( )
| A. | Na+ Ag+ OHˉ NO3- | B. | Na+ Cu2+ SO42- NO3- | ||
| C. | Mg2+ Na+ SO42- Cl- | D. | Ba2+ K+OH-HCO3- |
4.某化合物丙是药物中间体,其合成路线如下:
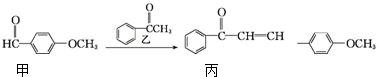
下列有关叙述不正确的是( )

下列有关叙述不正确的是( )
| A. | 丙的分子式为C16H14O2 | |
| B. | 丙分子中所有碳原子可能共平面 | |
| C. | 用酸性KMnO4溶液可区分甲和丙 | |
| D. | 乙在一定条件下最多与4mol氢气发生加成反应 |
11.下列说法中正确的是( )
| A. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| B. | 蔗糖、硫酸钡和水分别属于非电解质、弱电解质、弱电解质 | |
| C. | Mg、Cu、Fe均可以用直接焦炭加热还原法得到 | |
| D. | 煤、石油、天然气均属于化石能源 |
8.不能说明氯的非金属性比硫强的事实是( )
| A. | HCl受热不分解,H2S受热分解 | |
| B. | 往H2S溶液中通入氯气,生成硫和氯化氢 | |
| C. | 与Cu化合时,硫显-2价,氯显-1价 | |
| D. | Cl、S原子的电子层数相同,且Cl原子半径比S原子半径小 |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃时,pH=3的1.0LNaHSO3溶液中,含Na+数目为0.001 NA | |
| B. | 1 mol 明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA | |
| C. | 1 L 0.1 mol/L Na2CO3溶液中CO32-和HCO3-总数为0.1 NA | |
| D. | 标准状况下,11.2 L的乙烯中含有的共用电子对数为3NA |

 某离子晶体的晶胞结构如图所示.
某离子晶体的晶胞结构如图所示.