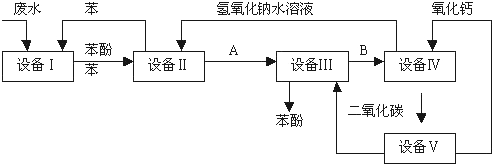
题目内容
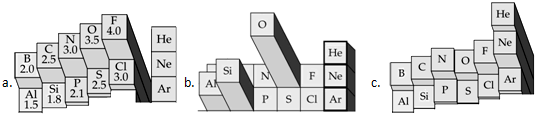
下表为长式周期表的一部分,其中的编号代表对应的元素.
(1)写出上表中元素⑩基态原子的外围电子排布图 .
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为: .
(3)按要求完成下列各题:
a.与元素④所形成的单质互为等电子体的分子、离子的化学式 、 (各一种).
b.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为 .
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子.0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.该反应的热化学方程式为 .
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: .
(6)元素⑨和铁元素均可形成+2价氧化物,晶体结构类型均与氯化铯的相同,
a、比较离子半径大小:Cl- K+(填“大于”、“小于”或“等于”).
b、元素⑨和铁的+2价离子半径分别为69pm和78pm,则比较两种氧化物的熔点较高的为 (填化学式),请解释原因 .
(7)元素⑩所形成的单质晶体中原子的堆积方式为fcc(面心立方),晶胞边长为361pm.又知⑩单质的密度为9.00g?cm-3,原子量为63.6,请回答下列问题:
a、晶体中该原子的配位数为 ,一个晶胞中包含的原子数目为 .
b、⑩单质的晶胞的体积是 cm3,阿伏加德罗常数为 (列式计算).
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:
(3)按要求完成下列各题:
a.与元素④所形成的单质互为等电子体的分子、离子的化学式
b.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子.0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.该反应的热化学方程式为
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:
(6)元素⑨和铁元素均可形成+2价氧化物,晶体结构类型均与氯化铯的相同,
a、比较离子半径大小:Cl-
b、元素⑨和铁的+2价离子半径分别为69pm和78pm,则比较两种氧化物的熔点较高的为
(7)元素⑩所形成的单质晶体中原子的堆积方式为fcc(面心立方),晶胞边长为361pm.又知⑩单质的密度为9.00g?cm-3,原子量为63.6,请回答下列问题:
a、晶体中该原子的配位数为
b、⑩单质的晶胞的体积是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知①为H,②为Li,③为C,④为N,⑤为O,⑥为F,⑦为Mg,⑧为S,⑨为Ni,⑩为Cu,
(1)⑩为Cu,原子序数为29,结合构造原理书写电子排布式;
(2)元素③与①形成的水果催熟剂为C2H4,根据形成的δ键判断;
(3)元素④所形成的单质为N2,含有14个电子;元素④的气态氢化物X为NH3,与H2O2反应生成N2和水;
(4)元素③和⑧形成的液态化合物CS2;
(5)HF分子之间因形成氢键而形成(HF)n缔合分子;
(6)a、核外电子排布相同的离子,核电荷数越大,离子半径越小;
b、离子半径越小、晶体熔点越高;
(7)利用均摊法计算.
(1)⑩为Cu,原子序数为29,结合构造原理书写电子排布式;
(2)元素③与①形成的水果催熟剂为C2H4,根据形成的δ键判断;
(3)元素④所形成的单质为N2,含有14个电子;元素④的气态氢化物X为NH3,与H2O2反应生成N2和水;
(4)元素③和⑧形成的液态化合物CS2;
(5)HF分子之间因形成氢键而形成(HF)n缔合分子;
(6)a、核外电子排布相同的离子,核电荷数越大,离子半径越小;
b、离子半径越小、晶体熔点越高;
(7)利用均摊法计算.
解答:
解:由元素在周期表中的位置可知①为H,②为Li,③为C,④为N,⑤为O,⑥为F,⑦为Mg,⑧为S,⑨为Ni,⑩为Cu,
(1)⑩为Cu,原子序数为29,电子排布式为1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)元素③与①形成的水果催熟剂为C2H4,结构简式为CH2=CH2,C形成3个δ键,为sp2杂化,故答案为:sp2;
(3)a、元素④所形成的单质为N2,含有14个电子,与元素④所形成的单质互为等电子体的分子、离子有CO、C22-或CN-或NO+或O22+,
故答案为:CO;C22-或CN-或NO+或O22+;
b、元素④的气态氢化物X为NH3,与H2O2反应生成N2和水,方程式为2NH3+3H2O2=N2+6H2O,故答案为:2NH3+3H2O2=N2+6H2O;
(4)元素③和⑧形成的液态化合物CS2,0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.
则1mol燃烧放出1075kJ,热化学方程式为CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-1075kJ/mol,
故答案为:CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-1075kJ/mol;
(5)F的非金属性很强,对应氢化物中含有氢键,HF分子之间因形成氢键而形成(HF)n缔合分子,实际测得的为HF和(HF)n的相对分子质量的平均值,比HF的分子量大,
故答案为:HF分子之间因形成氢键而形成(HF)n缔合分子,实际测得的为HF和(HF)n的相对分子质量的平均值,比HF的分子量大;
(6)a、Cl-、K+核外电子排布相同,核电荷数越大,离子半径越小,Cl的原子序数小于K,则Cl-离子半径较大,故答案为:大于;
b、两种氧化物中的阴阳离子的电荷(绝对值)均相等,离子半径越小、晶格能越大,则晶体熔点越高,
故答案为:NiO;两种氧化物中的阴阳离子的电荷(绝对值)均相等,Ni2+的半径小则NiO的阴阳离子核间距小于FeO的阴阳离子核间距,可知NiO的晶格能较大,熔点高;
(7)a、Cu单质的晶体为面心立方最密堆积,以顶点Cu原子研究,与之最近的Cu原子处于面心上,每个顶点为12个面共用,故Cu的配位数为12,
一个晶胞中包含的原子数目为6×
+8×
=4,
故答案为:12;4;
b、晶胞边长为361pm.则晶胞的体积为(361×10-10cm)3=4.70×10-23cm3,
设阿伏加德罗常数为NA,
则ρ=
=
=9.00g?cm-3,则NA=
/mol,
故答案为:4.70×10-23;NA=
/mol=6.01×1023mol-1.
(1)⑩为Cu,原子序数为29,电子排布式为1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)元素③与①形成的水果催熟剂为C2H4,结构简式为CH2=CH2,C形成3个δ键,为sp2杂化,故答案为:sp2;
(3)a、元素④所形成的单质为N2,含有14个电子,与元素④所形成的单质互为等电子体的分子、离子有CO、C22-或CN-或NO+或O22+,
故答案为:CO;C22-或CN-或NO+或O22+;
b、元素④的气态氢化物X为NH3,与H2O2反应生成N2和水,方程式为2NH3+3H2O2=N2+6H2O,故答案为:2NH3+3H2O2=N2+6H2O;
(4)元素③和⑧形成的液态化合物CS2,0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ.
则1mol燃烧放出1075kJ,热化学方程式为CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-1075kJ/mol,
故答案为:CS2(l)+3O2(g)═CO2(g)+2SO2(g)△H=-1075kJ/mol;
(5)F的非金属性很强,对应氢化物中含有氢键,HF分子之间因形成氢键而形成(HF)n缔合分子,实际测得的为HF和(HF)n的相对分子质量的平均值,比HF的分子量大,
故答案为:HF分子之间因形成氢键而形成(HF)n缔合分子,实际测得的为HF和(HF)n的相对分子质量的平均值,比HF的分子量大;
(6)a、Cl-、K+核外电子排布相同,核电荷数越大,离子半径越小,Cl的原子序数小于K,则Cl-离子半径较大,故答案为:大于;
b、两种氧化物中的阴阳离子的电荷(绝对值)均相等,离子半径越小、晶格能越大,则晶体熔点越高,
故答案为:NiO;两种氧化物中的阴阳离子的电荷(绝对值)均相等,Ni2+的半径小则NiO的阴阳离子核间距小于FeO的阴阳离子核间距,可知NiO的晶格能较大,熔点高;
(7)a、Cu单质的晶体为面心立方最密堆积,以顶点Cu原子研究,与之最近的Cu原子处于面心上,每个顶点为12个面共用,故Cu的配位数为12,
一个晶胞中包含的原子数目为6×
| 1 |
| 2 |
| 1 |
| 8 |
故答案为:12;4;
b、晶胞边长为361pm.则晶胞的体积为(361×10-10cm)3=4.70×10-23cm3,
设阿伏加德罗常数为NA,
则ρ=
| m |
| V |
4×
| ||
| 4.70×10-23 |
| 4×63.6 |
| 9.00×4.70×10-23 |
故答案为:4.70×10-23;NA=
| 4×63.6 |
| 9.00×4.70×10-23 |
点评:本题以元素推断为载体,综合考查物质结构与性质,涉及核外电子排布规律、杂化理论与分子结构、氢键、晶胞计算等,难度中等,(7)注意利用均摊法进行晶胞计算.

练习册系列答案
相关题目
下列说法正确的是( )
A、化合物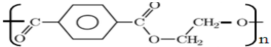 名称为聚对苯甲二酸乙二酯 名称为聚对苯甲二酸乙二酯 |
| B、C3H7OH与C4H9OH分子间脱水,最多可生成6种醚 |
C、1mol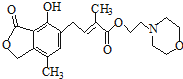 最多可与含4mol NaOH的水溶液完全反应 最多可与含4mol NaOH的水溶液完全反应 |
D、某油脂的化学式为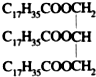 ,它属于酯类但不属于高分子化合物 ,它属于酯类但不属于高分子化合物 |
深秋及寒冬的清晨,我们安庆市经常出现大雾天气,雾中小液滴直径范围是( )
| A、小于1 nm |
| B、在1~100 nm间 |
| C、大于100 nm |
| D、无法确定 |
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质 |
| B、用渗析的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |