题目内容
氧、硫、氯是中学化学重点研究的非金属元素,回答下列问题:
(1)三种元素形成的常见氢化物中稳定性最差的是 ,沸点最高的是 ,其沸点最高的主要原因是 .
(2)硫单质与铁在加热时反应的方程式是 ,通过硫和氯的单质分别与铁的反应对比,从氧化还原角度可以得出的结论是 .
(1)三种元素形成的常见氢化物中稳定性最差的是
(2)硫单质与铁在加热时反应的方程式是
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题,元素及其化合物
分析:(1)元素的非金属性越强,对应的氢化物越稳定,且当氢化物含有氢键时,沸点较高;
(2)元素的非金属性越强,对应的单质的氧化性越强,氯气的氧化性比硫强,与铁反应时,分别生成氯化铁和硫化亚铁.
(2)元素的非金属性越强,对应的单质的氧化性越强,氯气的氧化性比硫强,与铁反应时,分别生成氯化铁和硫化亚铁.
解答:
解:(1)非金属性Cl和O相接近,而S的非金属性最小,元素的非金属性越强,对应的氢化物越稳定,则定性最差的是H2S,水中含有氢键,常温下为液体,沸点最高,
故答案为:H2S;H2O;水分子间存在氢键;
(2)硫的氧化性较氯气的弱,与铁反应生成硫化亚铁,反应的方程式为Fe+S═FeS,
故答案为:Fe+S═FeS;氯气的氧化性强于硫.
故答案为:H2S;H2O;水分子间存在氢键;
(2)硫的氧化性较氯气的弱,与铁反应生成硫化亚铁,反应的方程式为Fe+S═FeS,
故答案为:Fe+S═FeS;氯气的氧化性强于硫.
点评:本题考查元素的非金属性的比较,为高频考点,侧重于学生的分析能力的考查,注意把握元素的性质与对应单质、化合物的性质的关系,把握比较的角度和方法,难度不大.

练习册系列答案
相关题目
下列除杂方案中,括号内为除去杂质所需的药品,其中正确的是( )
| A、NaOH溶液中混有Ba(OH)2[K2SO4] |
| B、Cu(NO3)2溶液中混有AgNO3[Cu粉] |
| C、CO2中混有CO[炽热的炭] |
| D、CO2中混有HCl气体[NaOH溶液] |
金属钛对体液无毒且有惰性,能与肌肉和骨骼生长在一起,因而有“生命金属”之称.下列有关
Ti和
Ti的说法中正确的是( )
48 22 |
50 22 |
A、
| ||||
B、
| ||||
C、分别由
| ||||
D、
|
下列装置中电流表中有电流产生的是( )
A、 碳酸溶液 |
B、 氯化铁溶液 |
C、 稀盐酸 |
D、 酒精 |
下列反应速率(v)和温度(T)的关系示意图与铝热反应最接近的是( )
A、 |
B、 |
C、 |
D、 |
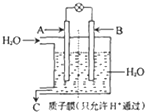 “温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.
“温室效应”是哥本哈根气候变化大会研究的环境问题之一.CO2是目前大气中含量最高的一种温室气体.因此,控制和治理CO2是解决“温室效应”的有效途径.