题目内容
5.已知卤代烃可以和钠发生反应,例如溴乙烷与钠反应为:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )| A. | CH3CH2Br | B. | CH3CH2CH2CH2Br | ||
| C. | CH2Br CH2CH2Br | D. | CH2Br CH2CH2CH2Br |
分析 由2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr可知,碳溴键发生断裂,溴原子与钠形成溴化钠,与溴原子相连的碳相连形成新的碳碳键,若形成环状结构,分子中一定含有两个溴原子,以此来解答.
解答 解:A.CH3CH2Br与钠以2:2发生反应,反应后生成的是CH3CH2CH2CH3,故A不选;
B.CH3CH2CH2CH2Br与钠以2:2发生反应,反应后生成的是CH3CH2CH2CH2CH2CH2CH2CH3,故B不选;
C.CH2BrCH2CH2Br与钠以1:2发生反应,反应生成环丙烷,故C不选;
D.CH2Br CH2CH2CH2Br与钠以1:2发生反应,反应后生成环丁烷,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意信息中取代反应发生时化学键的断裂,题目难度不大.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
16.下列说法不正确的是( )
| A. | O2和O3互为同素异形体 | |
| B. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H互为同位素 | |
| C. | CH2═CH2和 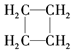 互为同系物 互为同系物 | |
| D. | 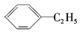 和 和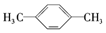 互为同分异构体 互为同分异构体 |
20.下列有关于氯及其化合物的说法不正确的是( )
| A. | 电解饱和食盐水可制得黄绿色的氯气 | |
| B. | 氢气在氯气中安静地燃烧,发出黄色火焰,生成物溶于水可制得盐酸 | |
| C. | 工业上用Cl2和石灰乳为原料制造漂白粉 | |
| D. | Cl2能与铁反应生成氯化铁 |
10.如图是部分短周期元素的化合价与原子序数的关系图,下列说法正确的是( )


| A. | 原子半径:R>W>Z>Y>X | |
| B. | 氧化物对应水化物的酸性:R>W | |
| C. | 气态氢化物的稳定性:W>X | |
| D. | Y、Z、W最高价氧化物对应水化物两两之间均能相互反应 |
14.下列反应的离子方程式书写不正确的是( )
| A. | 1.5mol/L100mL的FeI2溶液中,通入少量Cl2:2I-+Cl2=I2+2Cl- | |
| B. | 饱和的碳酸钠溶液中滴加少量稀盐酸:CO32-+H+=HCO3- | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| D. | 次氯酸钠溶液中通入少量的SO2气体:2ClO-+SO2+H2O=SO32-+2HClO |
16.下列离子方程式书写正确的是( )
| A. | 铜与氯化铁溶液反应:2Fe3++Cu═2Fe2++Cu2+ | |
| B. | 锌粒与稀硝酸反应:Zn+2 H+═Zn2++H2↑ | |
| C. | 氯气与水反应:H2O+Cl2═2H++Cl-+ClO- | |
| D. | 工业制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O |

