题目内容
14.下列反应的离子方程式书写不正确的是( )| A. | 1.5mol/L100mL的FeI2溶液中,通入少量Cl2:2I-+Cl2=I2+2Cl- | |
| B. | 饱和的碳酸钠溶液中滴加少量稀盐酸:CO32-+H+=HCO3- | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| D. | 次氯酸钠溶液中通入少量的SO2气体:2ClO-+SO2+H2O=SO32-+2HClO |
分析 A.还原性碘离子大于亚铁离子,少量氯气只氧化碘离子;
B.加少量盐酸反应生成氯化钠、碳酸氢钠;
C.反应生成氢氧化铝和氯化铵;
D.发生氧化还原反应生成硫酸钠.
解答 解:A.1.5mol/L100mL的FeI2溶液中,通入少量Cl2的离子反应为2I-+Cl2=I2+2Cl-,故A正确;
B.饱和的碳酸钠溶液中滴加少量稀盐酸的离子反应为CO32-+H+=HCO3-,故B正确;
C.氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C正确;
D.次氯酸钠溶液中通入少量的SO2气体的离子反应为SO2+3ClO-+H2O=2HClO+SO42-+Cl-,故D错误;
故选D.
点评 本题考查离子方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意与量有关的反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
4.下列叙述违背化学原理的是( )
| A. | NaHCO3溶液与NaAlO2溶液混合生成白色沉淀,说明结合H+的能力:AlO2->CO32- | |
| B. | 将SO2通入酸性KMnO4溶液中溶液褪色,不能说明SO2具有漂白性 | |
| C. | 工业上制钾的反应为Na+KCl (熔融)=NaCl+K↑,说明还原性Na比K强 | |
| D. | 亚硫酸是良好的还原剂,浓硫酸是良好的氧化剂,但两者混合,却不发生氧化还原反应 |
5.已知卤代烃可以和钠发生反应,例如溴乙烷与钠反应为:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr,应用这一反应,下列所给化合物中可以与钠合成环丁烷的是( )
| A. | CH3CH2Br | B. | CH3CH2CH2CH2Br | ||
| C. | CH2Br CH2CH2Br | D. | CH2Br CH2CH2CH2Br |
2.下列表达正确的是( )
| A. | 羟基的电子式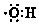 | B. | 醛基的结构简式-COH | ||
| C. | 2-丁烯的键线式  | D. | 2-丙醇的结构简式 C3H7-OH |
7.下列四组选项中,全部符合如图阴影部分的能源分类是( )


| A. | 太阳能、风能、潮汐能 | B. | 水能、生物质能、天然气 | ||
| C. | 煤炭、生物质能、沼气 | D. | 地热能、石油、核能 |
4.下列分子的电子式书写正确的是( )
| A. | 双氧水 | B. | 四氯化碳 | C. | 氮气 | D. | 二氧化碳  |
 某有机物由C、H、O三种元素组成,球棍模型如图所示:
某有机物由C、H、O三种元素组成,球棍模型如图所示: .
.