题目内容
在1L密闭容器中通入2mol氨气,在一定温度下发生反应;2NH3?N2+3H2,达平衡时,N2的物质的量分数为a%,维持容器的体积和温度不变,分别通入下列几组物质,达到平衡时,容器内N2的物质的量分数仍为a%的是( )
| A、3mol H2和1mol N2 |
| B、2mol NH3和1mol N2 |
| C、2mol N2和3mol H2 |
| D、1mol NH3、1mol N2、3mol H2 |
考点:等效平衡
专题:化学平衡专题
分析:此题考查判断全等平衡的方法,一般是将物质全部靠到一边进行极限转化,再与原反应进行比较来判断,若各物质与原来相等,则等效,否则不等效.
解答:
解:A、采用极限分析法,3molH2和1molN2反应生成NH3,假如反应完全,就会生成2molNH3,这和题目开始一样,故A正确;
B、2molNH3和1molN2,这和题目开始不一样,故B错误;
C、采用极限分析法,2molN2和3molH2反应生成NH3,假如反应完全,就会生成2molNH3,还有剩余的1molN2,这和题目开始不一样,故C错误;
D、采用极限分析法,1molN2和3molH2反应生成NH3,假如反应完全,就会生成2molNH3,在加上原来的molNH3,共3molNH3,这和题目开始不一样,故D错误;
故选:A.
B、2molNH3和1molN2,这和题目开始不一样,故B错误;
C、采用极限分析法,2molN2和3molH2反应生成NH3,假如反应完全,就会生成2molNH3,还有剩余的1molN2,这和题目开始不一样,故C错误;
D、采用极限分析法,1molN2和3molH2反应生成NH3,假如反应完全,就会生成2molNH3,在加上原来的molNH3,共3molNH3,这和题目开始不一样,故D错误;
故选:A.
点评:抓住判断全等平衡的方法,一般是将物质全部靠到一边进行极限转化,再与原反应进行比较来判断,若各物质与原来相等,则等效,否则不等效.

练习册系列答案
相关题目
用一定方法可除去下列物质所含的少量杂质(括号内为杂质).其中加适量的稀盐酸能达到除去杂质的目的是( )
| A、NaHCO3 (Na2CO3) |
| B、NaCl(NaOH) |
| C、Fe2O3(MgO) |
| D、FeCl3(FeCl2) |
相同温度下,相同物质的量浓度的七种溶液:①CH3COONa,②NaHSO4,③NaCl,④Na2CO3,⑤NaHCO3,⑥CH3COOH,⑦NH4Cl.按pH 由大到小的顺序排列正确的是( )
| A、⑤④①③⑦⑥② |
| B、②⑥⑦③①⑤④ |
| C、④⑤①③⑦⑥② |
| D、②⑥⑦③①④⑤ |
一定温度下,向一固定容积的容器中放入1mol A和1mol B,待反应A(s)+B(g)?C(g)+2D(g)达到平衡时,C的体积分数是M%,在相同的条件下,若按以下配比开始反应,平衡时C的体积分数比为M%的是( )
| A、2molA+2molB |
| B、1molD+2molC |
| C、2molD+1molA+1molB |
| D、1molA+0.5molB+0.5molC+1.0molD |
了解安全知识,可以更好的保护自己.下列做法正确的是( )
| A、用甲醛溶液浸泡水产品以延长保质期 |
| B、在饲料中添加“瘦肉精”以增加猪肉的瘦肉含量 |
| C、高层住房着火.立即打开所有门窗 |
| D、燃着的酒精灯不慎碰到,立即用湿布盖灭 |
下列水作为反应物参加的反应中:①钠与水反应 ②Na2O2与水反应 ③氟气与水反应 ④电解水.按照水的作用依次是只作氧化剂、只作还原剂、既作氧化剂又作还原剂、既不作氧化剂又不作还原剂顺序排列是( )
| A、①②③④ | B、①③④② |
| C、①④②③ | D、①④③② |
下列物质属于非电解质的是( )
| A、烧碱 | B、干冰 |
| C、金刚石 | D、75%的酒精 |
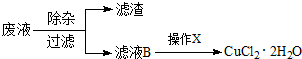
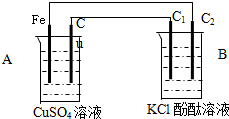 按如图装置进行实验,并回答下列问题:
按如图装置进行实验,并回答下列问题: