题目内容
15.某课外学习小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,先慢慢通入O2,一段时间后,再喷射蒸馏水即得硫酸型酸雨.则关于NO的作用说法正确的是( )| A. | 还原剂 | B. | 氧化剂 | C. | 反应物 | D. | 催化剂 |
分析 根据物质的性质来书写方程式,根据一氧化氮在反应中的特点来判断所起到的作用,由此分析解答.
解答 解:一氧化氮具有还原性,很容易被氧气氧化,反应的方程式为:2NO+O2=2NO2,二氧化氮能将二氧化硫氧化,反应的化学方程式为:NO2+SO2=SO3+NO,总反应为:2SO2+O2=2SO3,可见整个过程一氧化氮的质量没有变化,故NO在反应中作催化剂,
故选D.
点评 本题考查了催化剂,题目难度中等,试题涉及催化剂的概念、通过总反应方程来分析.

练习册系列答案
相关题目
5.关于重结晶的说法,错误的是( )
| A. | 被重结晶提纯的物质的溶解度随温度变化大 | |
| B. | 溶解度很小的杂质留在了热滤的滤渣里 | |
| C. | 重结晶的步骤为:加热溶解、冷却过滤、结晶 | |
| D. | 重结晶的首要工作是选择适当的溶剂 |
6.下列装置或操作正确且能达到实验目的是( )
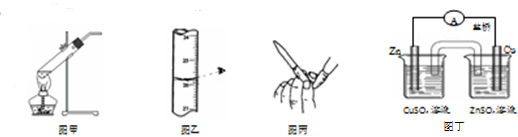

| A. | 用图甲所示装置加热分解NaHCO3固体 | |
| B. | 用图乙所示读取滴定管读数 | |
| C. | 用图丙所示排碱式滴定管尖嘴内的气泡 | |
| D. | 用图丁所示装置构成铜锌原电池 |
3.如图是Cu-Zn原电池的装置示意图,下列叙述正确的是( )
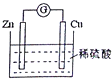

| A. | Zn片是正极 | |
| B. | 电池工作时,H+在铜片上得电子 | |
| C. | 电池工作时,电能转变为化学能,且锌片逐渐被消耗 | |
| D. | 电池工作时,电子从锌片通过硫酸溶液流向铜片 |
10.下列实验装置制取的是( )
| A. |  实验室制氨气 | B. |  实验室制乙烯 | ||
| C. |  实验室制氯气 | D. |  实验室制乙酸乙酯 |
20.下列涉及的实验方案或工业方案不能达到目的是( )
| A. | 用FeCl3溶液刻制铜材电路板 | |
| B. | 用乙醇作萃取剂从碘水中提取碘 | |
| C. | 在常温下用铝制容器贮运浓硫酸 | |
| D. | 向含硫高的煤中加入生石灰,可减少燃料对大气的污染 |
4.下列化学式只能表示一种物质的是( )
| A. | CH2Cl2 | B. | C2H4Cl2 | C. | C4H5 | D. | C5H12 |
 已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )
已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )