题目内容
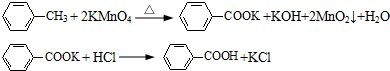
甲苯氧化法制备苯甲酸的反应原理如下:
实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100℃时,反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯.
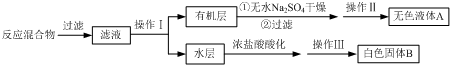

(1)实验室中实现操作Ⅰ所需的玻璃仪器有 、烧杯;操作Ⅱ的名称为 .
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是 .
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是 ;如图2所示抽滤完毕,应先断开 橡皮管.
(4)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为2.4×10-3 mol.产品中苯甲酸质量分数为 .

实验时将一定量的甲苯和KMnO4溶液置于图1装置中,在100℃时,反应一段时间,再停止反应,并按如下流程分离出苯甲酸和回收未反应的甲苯.


(1)实验室中实现操作Ⅰ所需的玻璃仪器有
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,若无此操作会出现的危害是
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,其原因是
(4)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定,消耗KOH物质的量为2.4×10-3 mol.产品中苯甲酸质量分数为
考点:物质分离、提纯的实验方案设计,有机物的合成,苯的同系物,探究物质的组成或测量物质的含量
专题:实验题,有机物的化学性质及推断
分析:一定量的甲苯和适量的KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液体采用分液方法分离,根据实验目的知,从而得到有机层和水层,有机层中含有甲苯、水层中含有苯甲酸,有机层中的甲苯采用蒸馏方法得到无色液体A,A是甲苯,将水层盐酸酸化再蒸发浓缩,根据苯甲酸的溶解度知,得到的固体B是苯甲酸,
(1)分离互不相溶的液体采用分液方法,分离互溶且沸点不同的液体采用蒸馏方法;
(2)如果滤液呈紫色,说明高锰酸钾过量,要先加亚硫酸氢钾,将高锰酸钾还原,否则浓盐酸可能被氧化成氯气;
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,可以得到较大的苯甲酸晶粒,便于抽滤,抽滤完毕,应先断开抽气泵和安全瓶之间的橡皮管;
(4)苯甲酸和KOH溶液发生酸碱中和反应,根据苯甲酸和KOH之间的关系式计算苯甲酸的质量,从而计算苯甲酸的质量分数.
(1)分离互不相溶的液体采用分液方法,分离互溶且沸点不同的液体采用蒸馏方法;
(2)如果滤液呈紫色,说明高锰酸钾过量,要先加亚硫酸氢钾,将高锰酸钾还原,否则浓盐酸可能被氧化成氯气;
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,可以得到较大的苯甲酸晶粒,便于抽滤,抽滤完毕,应先断开抽气泵和安全瓶之间的橡皮管;
(4)苯甲酸和KOH溶液发生酸碱中和反应,根据苯甲酸和KOH之间的关系式计算苯甲酸的质量,从而计算苯甲酸的质量分数.
解答:
解:一定量的甲苯和适量的KMnO4溶液在100℃反应一段时间后停止反应,按如图流程分离出苯甲酸和回收未反应的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液体采用分液方法分离,根据实验目的知,从而得到有机层和水层,有机层中含有甲苯、水层中含有苯甲酸,有机层中的甲苯采用蒸馏方法得到无色液体A,A是甲苯,将水层盐酸酸化再蒸发浓缩,根据苯甲酸的溶解度知,得到的固体B是苯甲酸,
(1)分离互不相溶的液体采用分液方法,根据流程图中,水层和有机层不互溶,所以可以采用分液方法分离,要用分液漏斗,有机层中物质互溶且沸点不同,所以可以采用蒸馏方法分离,
故答案为:分液漏斗;蒸馏;
(2)如果滤液呈紫色,说明高锰酸钾过量,要先加亚硫酸氢钾,将高锰酸钾还原,否则浓盐酸可能被氧化成氯气,
故答案为:过量的高锰酸钾氧化盐酸,产生氯气;
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,可以得到较大的苯甲酸晶粒,便于抽滤,抽滤完毕,应先断开抽气泵和安全瓶之间的橡皮管,
故答案为:得到较大的苯甲酸晶粒,便于抽滤;抽气泵和安全瓶;
(4)设苯甲酸的物质的量浓度为x,则25mL苯甲酸溶液中苯甲酸的物质的量=0.025xmol,
C6H5COOH+KOH→C6H5COOK+H2O
1mol 1mol
0.025xmol 2.40×10-3mol
1mol:1mol=0.025xmol:2.40×10-3mol
x=
=0.96,
则100mL苯甲酸中苯甲酸的质量=0.096mol/L×0.1L×122g/mol=1.1712g,
其质量分数=
=96%,
故答案为:96%.
(1)分离互不相溶的液体采用分液方法,根据流程图中,水层和有机层不互溶,所以可以采用分液方法分离,要用分液漏斗,有机层中物质互溶且沸点不同,所以可以采用蒸馏方法分离,
故答案为:分液漏斗;蒸馏;
(2)如果滤液呈紫色,说明高锰酸钾过量,要先加亚硫酸氢钾,将高锰酸钾还原,否则浓盐酸可能被氧化成氯气,
故答案为:过量的高锰酸钾氧化盐酸,产生氯气;
(3)在操作Ⅲ中,抽滤前需快速冷却溶液,可以得到较大的苯甲酸晶粒,便于抽滤,抽滤完毕,应先断开抽气泵和安全瓶之间的橡皮管,
故答案为:得到较大的苯甲酸晶粒,便于抽滤;抽气泵和安全瓶;
(4)设苯甲酸的物质的量浓度为x,则25mL苯甲酸溶液中苯甲酸的物质的量=0.025xmol,
C6H5COOH+KOH→C6H5COOK+H2O
1mol 1mol
0.025xmol 2.40×10-3mol
1mol:1mol=0.025xmol:2.40×10-3mol
x=
| 2.40×10-3mol×1mol |
| 1mol×0.025mol |
则100mL苯甲酸中苯甲酸的质量=0.096mol/L×0.1L×122g/mol=1.1712g,
其质量分数=
| 1.1712g |
| 1.220g |
故答案为:96%.
点评:本题考查混合物的分离和提纯,侧重考查分析问题能力、计算能力,明确物质的性质是解本题关键,知道根据物质的性质选取合适的分离方法,注意(4)中要计算100mL溶液中苯甲酸的质量,为易错点

练习册系列答案
相关题目
准确量取25.00mL KMnO4溶液于锥形瓶中并用某无色未知浓度的还原性A溶液进行滴定,所选仪器和指示剂均正确的是( )
| A、50 mL酸式滴定管;甲基橙 |
| B、50 mL碱式滴定管;酚酞 |
| C、50 mL量筒;石蕊 |
| D、50 mL酸式滴定管;不用指示剂 |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中正确的是( )
| A、氢氧燃料电池在碱性介质中的负极反应式:H2-2e-=2H+ | ||||
B、用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为:2C1-+2H2O
| ||||
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | ||||
| D、用镀层金属作阳极、镀件作阴极,进行电镀 |

 ),请在方框内写出合成路线流程(无机试剂任选).注:合成路线流程的书写格式参照如下示例:
),请在方框内写出合成路线流程(无机试剂任选).注:合成路线流程的书写格式参照如下示例:


