题目内容
海带成分中碘的检验实验方案设计
①取10g食用干海带,用刷子把干海带表面附着物刷净,不要用水洗.将海带剪碎,用酒精润湿放入瓷坩埚中,把坩埚置于泥三角上.用酒精灯灼烧盛有海带的坩埚,至海带完全烧成炭黑色灰后,停止加热,自然冷却.将坩埚内海带灰放至小烧杯中,再加入15mL蒸馏水,不断搅拌,煮沸4min~5min,使可溶物溶解,10分钟后过滤.将滤液分成四份放入试管中,并标为1、2、3、4号.
②在1号试管中滴入6滴稀硫酸后,再加入约3mL H2O2溶液,观察现象.滴入1%淀粉液1~2滴,观察现象.
③在2号试管中加入2mL新制的饱和氯水,振荡溶液,观察现象.2分钟后把加入氯水的溶液分成两份.其中甲中再滴入1%淀粉液1~2滴,观察现象.乙溶液中加入2mL CCl4,振荡萃取,静置2分钟后观察现象.
④在3号试管中加入食用碘盐3g,振荡使之充分溶解后滴入6滴稀硫酸.在滴入1%淀粉液1~2滴,观察现象.
⑤在4号试管中加入硝酸银溶液,振荡,再加入稀硝酸溶液. 原想利用反应Ag++I-=AgI↓生成黄色沉淀来检验碘离子.通过实验发现生成白色沉淀.用此方法检验碘元素失败.
完成下面的实验现象及分析
实验现象及分析
(5)导致第⑤步失败的可能原因是 .
(6)将AgCl白色沉淀加入到KI溶液中搅拌,看到的现象是沉淀由白色转化为黄色,说明Ksp(AgCl)>Ksp(AgI),“说明”正确吗? (填“正确”或“不正确”),理由是 .
①取10g食用干海带,用刷子把干海带表面附着物刷净,不要用水洗.将海带剪碎,用酒精润湿放入瓷坩埚中,把坩埚置于泥三角上.用酒精灯灼烧盛有海带的坩埚,至海带完全烧成炭黑色灰后,停止加热,自然冷却.将坩埚内海带灰放至小烧杯中,再加入15mL蒸馏水,不断搅拌,煮沸4min~5min,使可溶物溶解,10分钟后过滤.将滤液分成四份放入试管中,并标为1、2、3、4号.
②在1号试管中滴入6滴稀硫酸后,再加入约3mL H2O2溶液,观察现象.滴入1%淀粉液1~2滴,观察现象.
③在2号试管中加入2mL新制的饱和氯水,振荡溶液,观察现象.2分钟后把加入氯水的溶液分成两份.其中甲中再滴入1%淀粉液1~2滴,观察现象.乙溶液中加入2mL CCl4,振荡萃取,静置2分钟后观察现象.
④在3号试管中加入食用碘盐3g,振荡使之充分溶解后滴入6滴稀硫酸.在滴入1%淀粉液1~2滴,观察现象.
⑤在4号试管中加入硝酸银溶液,振荡,再加入稀硝酸溶液. 原想利用反应Ag++I-=AgI↓生成黄色沉淀来检验碘离子.通过实验发现生成白色沉淀.用此方法检验碘元素失败.
完成下面的实验现象及分析
实验现象及分析
| 试管号 | 加入试剂 | 实验现象 | 离子方程式 |
| 1号 | 稀硫酸、H2O2、淀粉液 | 溶液立刻由褐色变成蓝色 | (1) |
| 2号 甲 | 新制的饱和氯水、1%淀粉液 | (2) | 2I-+Cl2=I2+2Cl- |
| 2号 乙 | 新制的饱和氯水、CCl4 | (3) | |
| 3号 | 食用碘盐、稀硫酸、1%淀粉液 | 溶液立刻由无色变成蓝色 | (4) |
(6)将AgCl白色沉淀加入到KI溶液中搅拌,看到的现象是沉淀由白色转化为黄色,说明Ksp(AgCl)>Ksp(AgI),“说明”正确吗?
考点:氯、溴、碘的性质实验
专题:实验设计题
分析:海带中碘元素以I-的形式存在.
(1)H2O2在酸性环境下能将I-氧化为I2,据此写出离子方程式;
(2)氯水中的Cl2能将I-氧化为I2,而碘单质遇淀粉变蓝;
(3)氯水中的Cl2能将I-氧化为I2,而四氯化碳能将置换出的碘单质给从水溶液中萃取出来,由于四氯化碳密度比水大,据此分析萃取后的实验现象;
(4)食用碘盐中含KIO3,IO3-和I-在酸性条件下能发生归中反应,生成碘单质,据此写出离子方程式;
(5)海带中存在大量NaCl,生成的大量的白色沉淀能掩盖黄色沉淀;
(6)只要离子积Qc>Ksp即可生成沉淀.
(1)H2O2在酸性环境下能将I-氧化为I2,据此写出离子方程式;
(2)氯水中的Cl2能将I-氧化为I2,而碘单质遇淀粉变蓝;
(3)氯水中的Cl2能将I-氧化为I2,而四氯化碳能将置换出的碘单质给从水溶液中萃取出来,由于四氯化碳密度比水大,据此分析萃取后的实验现象;
(4)食用碘盐中含KIO3,IO3-和I-在酸性条件下能发生归中反应,生成碘单质,据此写出离子方程式;
(5)海带中存在大量NaCl,生成的大量的白色沉淀能掩盖黄色沉淀;
(6)只要离子积Qc>Ksp即可生成沉淀.
解答:
解:海带中碘元素以I-的形式存在.
(1)H2O2有强氧化性,I-有强还原性,H2O2在酸性环境下能将I-氧化为I2,H2O2被还原为H2O,离子方程式:2I-+2H++H2O2=I2+2H2O,故答案为:2I-+2H++H2O2=I2+2H2O;
(2)氯水中的Cl2能将I-氧化为I2,呈褐色,而碘单质遇淀粉变蓝,故现象为:溶液立刻由褐色变成蓝色;
(3)氯水中的Cl2能将I-氧化为I2,得碘水,而I2在有机溶剂中的溶解度大于在水中的溶解度,故四氯化碳能将碘单质给从水溶液中萃取出来.而四氯化碳密度比水大,据萃取后分层,碘的四氯化碳溶液在下层,为紫红色,水在上层,为无色,故答案为:溶液分成两层,上层为接近无色,下层呈现紫红色;
(4)食用碘盐中含KIO3,IO3-和I-在酸性条件下能发生归中反应,生成碘单质,离子方程式:5I-+IO3-+6H+=3I2+3H2O,故答案为:5I-+IO3-+6H+=3I2+3H2O;
(5)海带中存在大量NaCl,生成的大量的白色沉淀能掩盖黄色沉淀,故失败的原因可能是:海带中存在大量氯化钠,Ag++Cl-=AgCl↓,生成大量白色AgCl掩盖黄色了AgI沉淀,故答案为:海带中存在大量氯化钠,Ag++Cl-=AgCl↓,生成大量白色AgCl掩盖黄色了AgI沉淀;
(6)沉淀容易由Ksp大的向Ksp小的转化,但不是只能由Ksp大的向Ksp小的转化,因为只要离子积Qc>Ksp即可生成沉淀,故白色沉淀转化为黄色,不能说明Ksp(AgCl)>Ksp(AgI),故答案为:不正确;沉淀的转化不单单由Ksp的大小决定,只要Ksp表达式中各离子的浓度的幂乘积>对应的Ksp,就会发生沉淀的转化.
(1)H2O2有强氧化性,I-有强还原性,H2O2在酸性环境下能将I-氧化为I2,H2O2被还原为H2O,离子方程式:2I-+2H++H2O2=I2+2H2O,故答案为:2I-+2H++H2O2=I2+2H2O;
(2)氯水中的Cl2能将I-氧化为I2,呈褐色,而碘单质遇淀粉变蓝,故现象为:溶液立刻由褐色变成蓝色;
(3)氯水中的Cl2能将I-氧化为I2,得碘水,而I2在有机溶剂中的溶解度大于在水中的溶解度,故四氯化碳能将碘单质给从水溶液中萃取出来.而四氯化碳密度比水大,据萃取后分层,碘的四氯化碳溶液在下层,为紫红色,水在上层,为无色,故答案为:溶液分成两层,上层为接近无色,下层呈现紫红色;
(4)食用碘盐中含KIO3,IO3-和I-在酸性条件下能发生归中反应,生成碘单质,离子方程式:5I-+IO3-+6H+=3I2+3H2O,故答案为:5I-+IO3-+6H+=3I2+3H2O;
(5)海带中存在大量NaCl,生成的大量的白色沉淀能掩盖黄色沉淀,故失败的原因可能是:海带中存在大量氯化钠,Ag++Cl-=AgCl↓,生成大量白色AgCl掩盖黄色了AgI沉淀,故答案为:海带中存在大量氯化钠,Ag++Cl-=AgCl↓,生成大量白色AgCl掩盖黄色了AgI沉淀;
(6)沉淀容易由Ksp大的向Ksp小的转化,但不是只能由Ksp大的向Ksp小的转化,因为只要离子积Qc>Ksp即可生成沉淀,故白色沉淀转化为黄色,不能说明Ksp(AgCl)>Ksp(AgI),故答案为:不正确;沉淀的转化不单单由Ksp的大小决定,只要Ksp表达式中各离子的浓度的幂乘积>对应的Ksp,就会发生沉淀的转化.
点评:本题考查了海带中碘离子的检验和沉淀的相互转化,应注意沉淀容易由Ksp大的向Ksp小的转化,但不是只能由Ksp大的向Ksp小的转化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
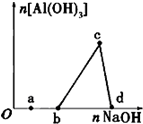 一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
一定量的酸性AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:K+、Ag+、Ca2+、NO3- |
| B、b点对应的溶液中:K+、NH4+、CO32-、SO42- |
| C、c点对应的溶液中:Na+、Fe3+、SO42-、HCO3- |
| D、d点对应的溶液中:Na+、S2-、SO42-、Cl- |
下列各组离子在指定条件下,一定能大量共存的是( )
| A、pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- |
| B、能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、NO3- |
| C、能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl- |
| D、水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- |
用惰性电极电解水时为了增强其导电性不应加入的是( )
| A、NaOH |
| B、CuSO4 |
| C、H2SO4 |
| D、KNO3 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1mol过氧化钠与水反应转移电子数为NA |
| B、0.1mol氯化铁水解制成胶体,所得胶体粒子数为0.1NA |
| C、标准状况下,22.4L水中含有水分子数为NA |
| D、1L 0.1mol每升乙酸溶液中氢离子数为0.1NA |

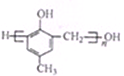 )的合成路线如下:
)的合成路线如下: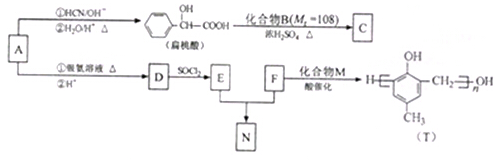
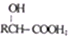

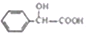 )有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有
)有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有