题目内容
7.下列说法正确的是( )| A. | 加大煤燃烧时与空气的接触面积,是为了获得更多的能量 | |
| B. | 钢铁易生锈被腐蚀,而铝、银等金属不容易被腐蚀,是因为铁的活泼性强 | |
| C. | 氢氧燃料电池把氢气和氧气燃烧放出的热能转化为电能 | |
| D. | 在实验室使用大理石与稀盐酸反应制取CO2,是为了控制CO2生成的速率 |
分析 A.增大接触面积是加快反应速率,一定量物质完全燃烧放出的热量一定;
B.钢铁易生锈被腐蚀主要是因为电化学腐蚀引起;
C.氢氧燃料电池是把化学能转化为电能;
D.大理石是块状固体,和盐酸在表面接触反应,浓度越小反应速率越慢;
解答 解:A.加大煤燃烧时与空气的接触面积,是为了反应更充分,增大反应速率,一定量物质完全燃烧放出的热量一定,不是为了获得更多的能量,故A错误;
B.钢铁易生锈被腐蚀主要是因为电化学腐蚀引起,而铝的表面有层氧化膜,阻止了它的氧化,银的活泼性差,故B错误;
C.氢氧燃料电池是反应中电子进行定向移动产生了电能,把化学能转化为电能,故C错误;
D.大理石是块状固体,和盐酸在表面接触反应,浓度越小反应速率越慢,使用大理石与稀盐酸反应制取CO2,可以控制CO2生成的速率,故D正确.
故选D.
点评 本题考查放热反应、电化学腐蚀、能量转化、反应速率等,题目难度不大,注意钢铁易生锈被腐蚀主要是因为电化学腐蚀引起.

练习册系列答案
相关题目
17.下列各组中的性质比较,不正确的是( )
| A. | 碱性:KOH>NaOH>Mg(OH)2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 稳定性:NH3<PH3<SiH4 | D. | 还原性:F-<Cl-<Br- |
18.组成和结构可用 表示的有机物共有(不考虑立体异构体)( )
表示的有机物共有(不考虑立体异构体)( )
 表示的有机物共有(不考虑立体异构体)( )
表示的有机物共有(不考虑立体异构体)( )| A. | 9种 | B. | 12种 | C. | 24种 | D. | 36种 |
15.烹鱼时加入少量食醋和料酒可以使烹制的鱼具有特殊的香味,这种香味来自于( )
| A. | 食盐 | |
| B. | 料酒中的乙醇和食醋中的乙酸反应生成的乙酸乙酯 | |
| C. | 料酒中的乙醇 | |
| D. | 食醋中的乙酸 |
12.一定条件下,有关金属腐蚀的下列说法不正确的是( )
| A. | 在酸性较强的溶液中,金属主要发生析氢腐蚀 | |
| B. | 钢铁制品吸氧腐蚀时正极反应:O2+2H2O+4e-═4OH- | |
| C. | 为减缓金属腐蚀,可将要保护的金属物件与外电源的正极相连接 | |
| D. | 在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀 |
19.下列化合物,既有离子键也有共价键的是( )
| A. | 氯化氢 | B. | 硫酸 | C. | 氯化铵 | D. | 乙酸 |
16.NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+═Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况.
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分,从而判断该消毒液是否变质.

限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI淀粉溶液、1.0mol•L-1 NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案.
(3)测定消毒液中NaClO的浓度.实验步骤如下:
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②定量分析.使c mol•L-1的酸性KMnO4溶液和剩余的Na2SO3发生反应.重复实验3次,测得平均消耗酸性KMnO4溶液V mL;此过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{(2ab-5vc)}{50}$mol•L-1(用含a、b、c、V的代数式表示).
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质.写出化学反应方程式:NaClO+CO2+H2O=NaHCO3+HClO.
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出.通过以下装置检验气体的成分,从而判断该消毒液是否变质.

限选试剂:98%浓硫酸、1%品红溶液、1.0mol•L-1 KI淀粉溶液、1.0mol•L-1 NaOH溶液、澄清石灰水、饱和NaCl溶液.
请完成下列实验方案.
| 所加试剂 | 预期现象和结论 |
| 向试管A中加足量①1.0 mol/L KI淀粉溶液;试管B中加1%品红溶液;试管C中加②澄清石灰水. | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质;③若A中溶液变蓝色,B中溶液不退色(无变化),C中溶液不变浑浊(无变化),则消毒液未变质,则消毒液未变质; ④若A中溶液不变蓝色(无变化),B中溶液不退色(无变化),C中溶液变浑浊则消毒液完变质,则消毒液完全变质. |
①量取25.00mL消毒液放入锥形瓶中,加入过量的a mol•L-1 Na2SO3溶液b mL.
②定量分析.使c mol•L-1的酸性KMnO4溶液和剩余的Na2SO3发生反应.重复实验3次,测得平均消耗酸性KMnO4溶液V mL;此过程中涉及的反应有:NaClO+Na2SO3═NaCl+Na2SO4;2KMnO4+5Na2SO3+3H2SO4═K2SO4+2MnSO4+5Na2SO4+3H2O.
③计算.消毒液中NaClO的浓度为$\frac{(2ab-5vc)}{50}$mol•L-1(用含a、b、c、V的代数式表示).
17.下列有关说法正确的是( )
| A. | 在轮船船体四周镶嵌锌块可以减少船体的腐蚀 | |
| B. | 通常情况下水分子较稳定是因为水分子间存在氢键 | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)(△H>0),其他条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动 | |
| D. | 相同温度下pH均为5的氯化铵溶液和醋酸溶液中水的电离程度相同 |
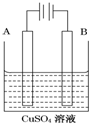 在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答: