题目内容
12.一定条件下,有关金属腐蚀的下列说法不正确的是( )| A. | 在酸性较强的溶液中,金属主要发生析氢腐蚀 | |
| B. | 钢铁制品吸氧腐蚀时正极反应:O2+2H2O+4e-═4OH- | |
| C. | 为减缓金属腐蚀,可将要保护的金属物件与外电源的正极相连接 | |
| D. | 在海轮外壳上附着一些锌块,则可以减缓海轮外壳的腐蚀 |
分析 A.酸性条件下,形成的原电池正极上氢离子得电子;
B.吸氧腐蚀是在形成的原电池正极上氧气得电子;
C.与原电池的正极相连作阳极,被腐蚀;
D.形成原电池时,活泼性强的被腐蚀.
解答 解:A.酸性条件下,正极上氢离子得电子,则在酸性较强的溶液中,金属主要发生析氢腐蚀,故A正确;
B.吸氧腐蚀时正极上氧气得电子,则钢铁制品腐蚀时正极反应:O2+2H2O+4e-=4OH-,故B正确;
C.与原电池的正极相连作电解池阳极被腐蚀,为减缓金属腐蚀,可将要保护的金属物件与外电源的负极相连接,与正极相连不能被保护,故C错误;
D.形成原电池时,活泼性强的被腐蚀,则在海轮外壳上附着一些锌块,形成原电池时Zn被腐蚀,铁被保护,所以可以减缓海轮外壳的腐蚀,故D正确.
故选C.
点评 本题考查金属的电化学腐蚀与防护,题目难度不大,本题注意电化学腐蚀形成的条件与金属的防护.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
2. 如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构.下列有关说法正确的是( )
如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构.下列有关说法正确的是( )
 如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构.下列有关说法正确的是( )
如图表示球棍模型,小球表示原子序数小于10的原子,短线表示化学键,每个原子都到达稳定结构.下列有关说法正确的是( )| A. | M分子的所有原子共面 | |
| B. | 0.1mol/L的N溶液中H+的物质的量浓度为0.1mol/L | |
| C. | L 存在同分异构体 | |
| D. | M、L都是烃类 |
3.230Th和 232Th是钍的两种同位素,232Th可以转化成 233U.下列有关Th的说法正确的是( )
| A. | Th元素的质量数是232 | B. | Th 元素的相对原子质量是231 | ||
| C. | 232Th 转化成 233U是化学变化 | D. | 230Th和 232Th的化学性质相同 |
20.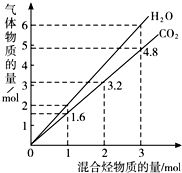 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
①一定有乙烯 ②一定有甲烷 ③一定有丙烷
④一定没有乙烷 ⑤可能有甲烷 ⑥可能有乙炔.
 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )①一定有乙烯 ②一定有甲烷 ③一定有丙烷
④一定没有乙烷 ⑤可能有甲烷 ⑥可能有乙炔.
| A. | ②⑤⑥ | B. | ②⑥ | C. | ②④ | D. | ②③ |
7.下列说法正确的是( )
| A. | 加大煤燃烧时与空气的接触面积,是为了获得更多的能量 | |
| B. | 钢铁易生锈被腐蚀,而铝、银等金属不容易被腐蚀,是因为铁的活泼性强 | |
| C. | 氢氧燃料电池把氢气和氧气燃烧放出的热能转化为电能 | |
| D. | 在实验室使用大理石与稀盐酸反应制取CO2,是为了控制CO2生成的速率 |
4.实验室里利用以下反应制取少量氮气:NaNO2+NH4Cl═NaCl+N2↑+2H2O.关于该反应的下列说法错误的是( )
| A. | NaNO2是氧化剂 | |
| B. | 氧化剂与还原剂物质的量之比为1:1 | |
| C. | NH4Cl中的氮元素被氧化 | |
| D. | 每生成1 mol N2转移的电子的物质的量为6 mol |
1.下列互为同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 氧气和臭氧 | C. | 正丁烷和正戊烷 | D. | 金刚石和石墨 |
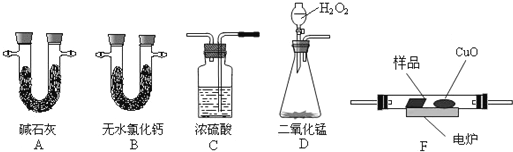
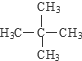 ;该有机物的一氯代物有1种,该有机物的二氯代物有2种.
;该有机物的一氯代物有1种,该有机物的二氯代物有2种.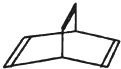 有机物的结构可用“键线式”简化表示,如:CH3一CH=CH-CH3可表示为
有机物的结构可用“键线式”简化表示,如:CH3一CH=CH-CH3可表示为 ,有一种有机物X的键线式如图所示.
,有一种有机物X的键线式如图所示. ;
;