题目内容
下列有关Fe2(SO4)3溶液的叙述正确的是( )
| A、该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| C、1 L 0.1 mol?L-1该溶液和足量的Zn充分反应,生成11.2 g Fe |
| D、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
考点:铁盐和亚铁盐的相互转变
专题:几种重要的金属及其化合物
分析:A.Fe3+与C6H5OH发生显色反应;
B.得失电子不守恒;
C.1 L 0.1 mol/L的该溶液中含有n(Fe3+)=1 L×0.2 mol/L=0.2 mol,利用原子守恒可知加入足量锌可置换出铁的质量为0.2 mol×56 g/mol=11.2 g;
D.离子方程式中离子不符合化学式的配比.
B.得失电子不守恒;
C.1 L 0.1 mol/L的该溶液中含有n(Fe3+)=1 L×0.2 mol/L=0.2 mol,利用原子守恒可知加入足量锌可置换出铁的质量为0.2 mol×56 g/mol=11.2 g;
D.离子方程式中离子不符合化学式的配比.
解答:
解:A.Fe3+与C6H5OH发生显色反应,不能共存,故A错误;
B.Fe2(SO4)3和KI溶液反应的离子方程式:2Fe3++2I-═2Fe2++I2,故B错误;
C.1 L 0.1 mol/L的该溶液中含有n(Fe3+)=1 L×0.2 mol/L=0.2 mol,利用原子守恒可知加入足量锌可置换出铁的质量为0.2 mol×56 g/mol=11.2 g,故C正确;
D.Fe2(SO4)3和Ba(OH)2溶液反应的离子方程式:2Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓,故D错误;
故选:C.
B.Fe2(SO4)3和KI溶液反应的离子方程式:2Fe3++2I-═2Fe2++I2,故B错误;
C.1 L 0.1 mol/L的该溶液中含有n(Fe3+)=1 L×0.2 mol/L=0.2 mol,利用原子守恒可知加入足量锌可置换出铁的质量为0.2 mol×56 g/mol=11.2 g,故C正确;
D.Fe2(SO4)3和Ba(OH)2溶液反应的离子方程式:2Fe3++3SO42-+3Ba2++6OH-=3BaSO4↓+2Fe(OH)3↓,故D错误;
故选:C.
点评:本题考查了离子方程式的书写、离子的共存,题目难度中等,明确反应的实质是书写离子方程式的关键,明确离子反应的条件是判断离子共存的关键,注意相关知识的积累.

练习册系列答案
相关题目
 H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )
H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )| A、1:1:1 |
| B、5:3:2 |
| C、2:1:5 |
| D、3:2:2 |
下列说法不正确的是( )
| A、可逆反应在一定条件下有一定的限度,当反应进行到一定限度后,反应物不再转化为生成物 |
| B、决定化学反应速率的主要因素是参加反应的物质的性质 |
| C、化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D、化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释不正确的是( )
| A、某溶液中加入稀硫酸再加入铜粉,共热,铜粉溶解且有红棕色气体产生,说明原溶液中含有NO3- |
| B、浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸 |
| C、某溶液中加入NaOH溶液,加热能产生使湿润的红色石蕊试纸变蓝的气体,说明原溶液中含有NH4+ |
| D、在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应 |
有机物A和B是正处于临床试验阶段的小分子抗癌药物,结构如图所示,关于有机物A和B的叙述,正确的是( )
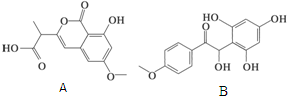

| A、二者都能与Br2发生反应,等物质的量A和B最多消耗的Br2的比例为2:3 |
| B、有机物A和B既可以与FeCl3溶液发生显色反应,又可以和NaHCO3溶液反应 |
| C、1 mol B最多能与6 mol氢气反应 |
| D、等物质的量A和B最多消耗的氢氧化钠质量比为1:1 |
关于NaHCO3的性质,下列说法正确的是( )
| A、和酸反应放出等量的CO2所消耗的酸比Na2CO3多 |
| B、相同温度下溶解度比Na2CO3要大 |
| C、热稳定性比Na2CO3小 |
| D、NaHCO3只能和酸作用不能和碱作用 |
下面的排序不正确的是( )
| A、晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B、晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C、硬度由大到小:金刚石>碳化硅>晶体硅 |
| D、熔点由高到低:Na>Mg>Al |