题目内容
 H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )
H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为( )| A、1:1:1 |
| B、5:3:2 |
| C、2:1:5 |
| D、3:2:2 |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:依次发生反应:H++OH-=H2O,Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,然后发生反应Al(OH)3+OH-═AlO2-+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为1mL,根据离子方程式Al3++3OH-═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的体积是3mL,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液5mL,计算沉淀Mg2+消耗的氢氧化钠溶液的体积2mL,氢离子消耗氢氧化钠1mL,据此确定溶液中n(Mg2+):n(Al3+):n(SO42-).
解答:
解:依次发生反应H++OH-=H2O、Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓,然后发生反应Al(OH)3+OH-═AlO2-+2H2O,由图可知,溶解Al(OH)3消耗氢氧化钠溶液的体积为1mL,根据离子方程式Al3++3OH-═Al(OH)3↓可知,沉淀Al3+消耗的氢氧化钠溶液的体积为1mL×3=3mL,沉淀Mg2+、Al3+总共消耗氢氧化钠溶液5mL,则沉淀Mg2+消耗的氢氧化钠溶液的体积为5mL-3mL=2mL,反应H++OH-=H2O,中和氢离子消耗氢氧化钠是1mL,则n(H+):n(Mg2+):n(Al3+)=1:(
×2mL):(
×3mL)=1:1:1,所H2SO4、Al2(SO4)3和MgSO4的物质的量之比为0.5:0.5:1,原混合溶液中Al3+、Mg2+和SO42-的物质的量之比为1:
:
=2:1:5.
故选C.
| 1 |
| 2 |
| 1 |
| 3 |
| 1 |
| 2 |
| 5 |
| 2 |
故选C.
点评:本题考查镁铝化合物性质、混合物的有关计算,难度中等,根据清楚图象反应过程是解题关键.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
150℃、101kPa时,由两种烃组成的混合气体0.5L在4.5L O2中完全燃烧,测得反应后气体总体积小于5L,其中含CO2 0.8L,则生成水蒸汽的体积为( )
| A、0.7 L |
| B、1.4 L |
| C、1.6 L |
| D、2.8 L |
某些芳香族化合物的分子式均为C7H8O,其中液态时能与金属Na反应产生H2和不反应产生H2的结构分别有( )
| A、2种和1种 |
| B、2种和3种 |
| C、3种和2种 |
| D、4种和1种 |
海洋中有丰富的食品、矿产、能源、药物和水产资源等,下列有关说法正确的是( )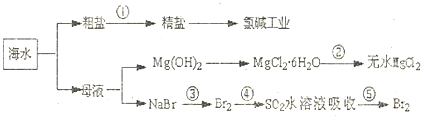
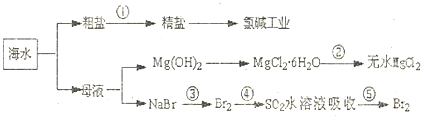
| A、流程①中除去粗盐中的SO42-,Ca2+,Mg2+,Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B、流程②中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在流程③④⑤中溴元素均被氧化 |
| D、大量的氮、磷废水排入海洋,易引发赤潮 |
能在有机物的分子中引入羟基的反应类型有:①酯化反应;②取代反应;③消去反应;④加成反应;⑤水解反应;⑥还原反应.其中正确的组合有( )
| A、①②③ | B、②④⑤ |
| C、②④⑤⑥ | D、②③④⑤⑥ |
下列有关Fe2(SO4)3溶液的叙述正确的是( )
| A、该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| C、1 L 0.1 mol?L-1该溶液和足量的Zn充分反应,生成11.2 g Fe |
| D、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |