题目内容
17. 近年来江南地区多次发生断肠草被当作“金银花”误食而使人中毒致死的事件.断肠 草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构简式.下列有关说法正确的是( )
近年来江南地区多次发生断肠草被当作“金银花”误食而使人中毒致死的事件.断肠 草为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构简式.下列有关说法正确的是( )| A. | ②中所含官能团种类比③中多 | |
| B. | ①、④互为同系物 | |
| C. | ①、②、③、④均由C、H、O三种元素组成 | |
| D. | 等物质的量的②、③分别在足量氧气中完全燃烧,前者消耗氧气比后者少 |
分析 A.②、③都含有醚基、碳碳双键、酯基等官能团;
B.结构相似,组成相差n个CH2原子团的化合物,互为同系物;
C.根据结构简式确定;
D.②比③多1个甲氧基.
解答 解:A.②、③都含有醚基、碳碳双键、酯基等官能团,所含官能团种类相等,故A错误;
B.同系物是指结构相似,分子式相差一个或若干个CH2原子团,①与④相差一个甲氧基,故不能互为同系物,故B错误;
C.由结构简式可知①、②、③、④均含有酯基,则均由C、H、O三种元素组成,故C正确;
D.②、③相比,②中多1个甲氧基,则等物质的量②、③分别在足量氧气中完全燃烧,前者消耗氧气比后者多,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酯性质和同分异构体、同系物的考查,题目难度中等,注意结构上的区别.

练习册系列答案
相关题目
7.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由苯硝化制硝基苯;由乙醇氧化制乙醛 | |
| C. | 由乙酸和乙醇制乙酸乙酯;由乙酸乙酯水解制乙醇 | |
| D. | 由氯代乙烷制乙烯;由丙烯制1,2-二溴丙烷 |
8.下列系统命名法正确的是( )
| A. | 2-甲基-4-乙基戊烷 | B. | 3,4-二乙基-4-戊烯 | ||
| C. | 2-甲基-3-丁炔 | D. | 对二甲苯 |
5.下列关于元素周期表的说法正确的是( )
| A. | 元素周期表是按照元素相对原子质量大小排列而成的 | |
| B. | 元素周期表有7个横行,也是7个周期;有18个纵行,即18个族 | |
| C. | 凡是位于元素周期表中同一周期的元素,都是按从左到右的顺序原子最外层电子数由1递增到8 | |
| D. | 凡是位于元素周期表中同一主族的元素,都是按从上到下的顺序电子层数逐渐增多 |
6.下列说法正确的是( )
| A. | 22.4L N2的物质的量为1mol | |
| B. | 标准状况下,1mol任何物质的体积为22.4L | |
| C. | SO2的摩尔质量与相对分子质量相等 | |
| D. | 在相同温度、压强下,相同体积的任何气体分子数相同 |
 .
.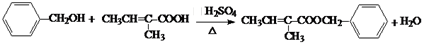 .
.
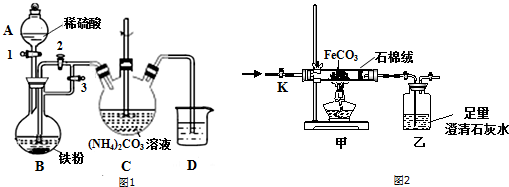
 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题:
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应.乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去,再与溴水反应.请你回答下列问题: