题目内容
5.标准状况下,由A、B两种气体组成的混合气体密度为1.5g/L,则A、B可能为( )| A. | H2和NH3 | B. | N2和O2 | C. | CO和CO2 | D. | H2S和HCl |
分析 根据M=ρVm计算平均摩尔质量,成分气体摩尔质量应一个大于,一个小于平均摩尔质量,或者都等于平均摩尔质量,据此分析解答.
解答 解:标准状况下,由A、B两种气体组成的混合气体密度为1.5g/L,则其平均摩尔质量为1.5g/L×22.4L/mol=33.6g/mol,
A.氢气和氨气摩尔质量都小于33.6g/mol,不符合题意,故A错误;
B.氮气和氧气摩尔质量都小于33.6g/mol,不符合题意,故B错误;
C.一氧化碳平均摩尔质量为28g/mol,二氧化碳平均摩尔质量为44g/mol,符合题意,故C正确;
D.硫化氢和氯化氢摩尔质量都大于33.6g/mol,不符合题意,故D错误;
故选:C.
点评 本题考查混合物计算,注意理解掌握标况下摩尔质量、密度与气体摩尔体积的关系,题目难度不大.

练习册系列答案
相关题目
15. 如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法不正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法不正确的是( )
 如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法不正确的是( )
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法不正确的是( )| A. | Na2O2中阴阳离子数目之比为1:2 | |
| B. | 反应①的离子方程式为:Na+2H2O═Na++2OH-+H2↑ | |
| C. | 反应③最多能产生0.05 mol O2 | |
| D. | ①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③ |
13.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是( )
| A. | 铁与氯气反应制氯化铁,推出铁与碘反应制碘化铁 | |
| B. | CO2通入到漂白粉溶液中发生CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推出SO2通入到漂白粉溶液中发生SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO | |
| C. | Na2O2与CO2反应生成Na2CO3和O2,推出Na2O2与SO2反应可生成Na2SO3和O2 | |
| D. | 利用可溶性的铝盐溶液与氨水反应制Al(OH)3,推出可溶性的铁盐溶液与氨水反应制Fe(OH)3 |
20.下列有关气体摩尔体积的描述中正确的是( )
| A. | 相同物质的量的气体摩尔体积也相同 | |
| B. | 通常状况下的气体摩尔体积约为22.4 L | |
| C. | 标准状况下的气体摩尔体积约为22.4 L/mol | |
| D. | 一定物质的量的气体所占的体积就是气体摩尔体积 |
10.高锰酸钾(KMnO4)是一种强氧化剂,在化学实验中被大量使用,下列关于它的性质和用途的叙述正确的是( )
| A. | 为了增强其氧化性,在配制时加入一定浓度的盐酸 | |
| B. | 该物质在反应中可以被还原,也可以被氧化 | |
| C. | 可用酸化的KMnO4溶液可以鉴别甲烷和乙烯 | |
| D. | KMnO4中Mn元素为其最高价+7,故含有最高价元素的化合物,均有强氧化性 |
17.常温下,下列各组离子在溶液中一定能大量共存的是( )
| A. | Fe3+、NO3-、SO42-、Na+ | B. | Ca2+、H+、Cl-、HCO3- | ||
| C. | NH4+、Al3+、NO3-、OH- | D. | Ba2+、ClO-、SO42-、SCN- |
15.在100ml 0.5mol/L的CuCl2溶液中含有Cl-的数目为( )
| A. | 6.02×1023 | B. | 6.02×1022 | C. | 6.02×1021 | D. | 6.02×1020 |
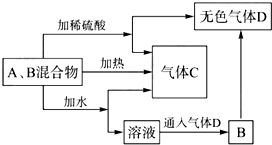 有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:
有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题: