题目内容
17.常温下,下列各组离子在溶液中一定能大量共存的是( )| A. | Fe3+、NO3-、SO42-、Na+ | B. | Ca2+、H+、Cl-、HCO3- | ||
| C. | NH4+、Al3+、NO3-、OH- | D. | Ba2+、ClO-、SO42-、SCN- |
分析 如离子之间不发生复分解反应生成沉淀、气体、水等,则可大量共存,以此解答该题.
解答 解:A.离子之间不反应,在溶液中能够大量共存,故A正确;
B.Ca2+、HCO3-反应生成二氧化碳和水,不能大量共存,故B错误;
C.NH4+、OH-之间发生反应,Al3+、OH-之间发生反应,在溶液中不能大量共存,故C错误;
D.Ba2+、SO42-反应生成沉淀而不能大量共存,故D错误.
故选A.
点评 本题考查离子共存,为高考常见题型,注意把握常见离子反应的类型:发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等,试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力及灵活应用能力.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
7.下述事实能够说明硫原子得电子能力比氯弱的是( )
| A. | 硫酸比盐酸稳定 | B. | 氯化氢比硫化氢稳定 | ||
| C. | 盐酸酸性比氢硫酸强 | D. | 亚硫酸酸性比高氯酸弱 |
8.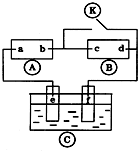 如图
如图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通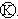 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )
 如图
如图 为直流电源,
为直流电源,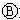 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,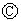 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现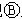 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )| A. | a为直流电源的负极 | B. | c极发生的反应为2H++2e-=H2↑ | ||
| C. | f电极为锌板 | D. |  中溶液的溶质为FeSO4 中溶液的溶质为FeSO4 |
5.标准状况下,由A、B两种气体组成的混合气体密度为1.5g/L,则A、B可能为( )
| A. | H2和NH3 | B. | N2和O2 | C. | CO和CO2 | D. | H2S和HCl |
12.对如图两种化合物的结构或性质描述正确的是( )
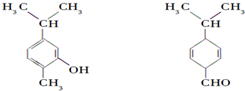
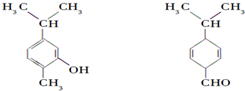
| A. | 不是同分异构体 | |
| B. | 分子中共平面的碳原子数相同 | |
| C. | 均能与H2在一定条件下发生加成反应 | |
| D. | 可用红外光谱区分,但不能用核磁共振氢谱区分 |
2.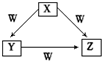 X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
 X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | O2 |
| B | Na | Na2O | Na2O2 | O2 |
| C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
| D | Fe | FeCl2 | FeCl3 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
7.根据热化学方程式:S(g)+O2(g)═SO2(g)△H=-Q kJ•mol-1(Q>0),则下列分析正确的是( )
| A. | 1mol S(g) 与1mol O2(g)的总能量比1mol SO2(g)的总能量低Q kJ | |
| B. | 1mol S(g) 与1mol O2(g)反应生成1mol SO2(g)放出Q kJ 的能量 | |
| C. | S(s)+O2(g)═SO2(g)△H<-Q kJ•mol-1 | |
| D. | 1个 S(g) 与1个 O2(g)完全反应可放出 Q kJ的能量 |
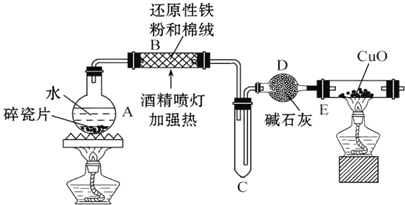 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题: