题目内容
14.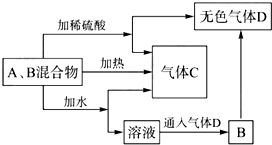 有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:
有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:(1)写出A的电子式

(2)①加热B产生D的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
②B加稀硫酸产生D的离子方程式HCO3-+H+=H2O+CO2↑
(3)请用化学方程式表示A在潜水艇中的一种重要用途2Na2O2+2CO2═2Na2CO3+O2
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E
①E的化学式为Na2CO3
②若只加入0.5a mol某一纯净物可将只含a mol B的溶液转变成只含a mol E的溶液,则该纯净物化学式为Na2O2或者Na2O.
分析 化合物A、B的焰色反应呈黄色,则A、B为钠的化合物.由A与B的混合物与水或硫酸反应产生气体C,可知混合物中必含有Na2O2,且C为O2.又因为加热A与B的混合物产生O2,说明另一物质的分解产物必有H2O和CO2,即另一种物质为NaHCO3.A与B的混合物溶于水的产物与D反应生成B,则B为NaHCO3,D为CO2,A为Na2O2,再结合题目分析解答.
解答 解:化合物A、B的焰色反应呈黄色,则A、B为钠的化合物.由A与B的混合物与水或硫酸反应产生气体C,可知混合物中必含有Na2O2,且C为O2.又因为加热A与B的混合物产生O2,说明另一物质的分解产物必有H2O和CO2,即另一种物质为NaHCO3.A与B的混合物溶于水的产物与D反应生成B,则B为NaHCO3,D为CO2,A为Na2O2,
(1)通过以上分析知,A为Na2O2,其电子式是 ,故答案为:
,故答案为: ;
;
(2)①NaHCO3加热分解生成碳酸钠、二氧化碳与水,反应方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
②NaHCO3与稀硫酸反应生成硫酸钠、二氧化碳与水,反应离子方程式为:HCO3-+H+=H2O+CO2↑,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;HCO3-+H+=H2O+CO2↑;
(3)过氧化钠可以作为潜水艇中的供氧剂,反应方程式为:2Na2O2+2CO2═2Na2CO3+O2,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(3)①NaHCO3、Na2O2在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为Na2CO3,
故答案为:Na2CO3;
②B为NaHCO3,E为Na2CO3,若只加入0.5a mol某一纯净物可将只含a mol B的溶液转变成只含a mol E的溶液,则该纯净物化学式为Na2O2 或者Na2O,
故答案为:Na2O2 或者Na2O.
点评 本题考查无机物的推断,涉及Na元素化合物性质与相互转化,难度中等,关键是根据焰色反应推断含有Na元素,再结合混合物与水、酸反应都去气体生成确定一定含有过氧化钠.

| A. | 常温常压下,0.5molH2中含有的H原子数 | |
| B. | 22.4升HCl气体中含有的Cl原子 | |
| C. | 1L1mol/L硫酸溶液所含的H+数 | |
| D. | 0.1mol金属铝含有的电子数 |
| A. | H2和NH3 | B. | N2和O2 | C. | CO和CO2 | D. | H2S和HCl |
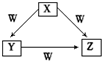 X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )
X、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是( )| X | Y | Z | W | |
| A | C | CO | CO2 | O2 |
| B | Na | Na2O | Na2O2 | O2 |
| C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
| D | Fe | FeCl2 | FeCl3 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 一氧化碳在氧气中的燃烧是吸热反应 |
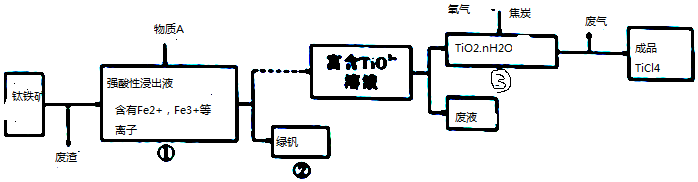
(1)FeTiO3中,Ti元素的化合价为+4.
(2)往①中加入的物质A是Fe.
(3)②中的绿矾带有棕黄色,原因可能是含有Fe3+;设计实验证明Fe3+杂质离子的存在取样,溶于水,向溶液中加入KSCN溶液,如果溶液变为血红色,证明含有Fe3+;
(4)写出③中TiO2和过量焦炭、氯气在高温下反应的化学方程式:TiO2+2C+Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.
(5)用金属Mg还原成品TiO4得到Mg、MgCl2和Ti的混合物,再真空蒸馏制备Ti. 依据下表,蒸馏温度略高于1412℃即可.
| Mg | MgCl2 | Ti | |
| 熔点/℃ | 648.0 | 714 | 1667 |
| 沸点/℃ | 1090 | 1412 | 3287 |
(7)向含有Fe2+、Fe3+溶液加入适量KOH和油脂,在高速撞拌下得到磁流体材料KxFeO2.
①若x=l.请写出在酸性条件下KxFeO2溶液与足量KI溶液反应的离子方程式:8H++2FeO2-+2I-=2Fe2++I2+4H2O.
②磁流体材料KxFeO2在组成上可理解为aK2O•bFeO•cFe2O3,若x=1.3,则b:c=6:7.
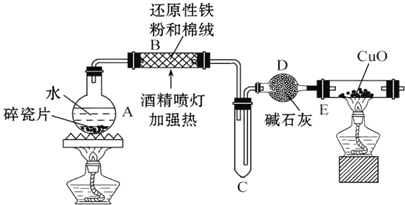 某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题: