题目内容
2.下列离子方程式正确的是( )| A. | 过量铁粉溶于稀HNO3中:Fe+NO3-+4H+═Fe3++NO↑+2H2O | |
| B. | 过量NaHSO4溶液加入到Ba(OH)2溶液中:2H++SO42-+Ba2++2 OH-═2H2O+BaSO4↓ | |
| C. | 少量Cl2通人FeBr2溶液中:2 Br-+Cl2═2 Cl-+Br2 | |
| D. | 少量 AlCl3溶液滴入到氨水中:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
分析 A.铁粉过量,反应生成的是亚铁离子;
B.硫酸氢钠过量,离子方程式按照氢氧化钡的化学式组成书写;
C.亚铁离子的还原性大于溴离子,氯气少量时亚铁离子优先反应;
D.氨水为弱碱,二者反应生成氢氧化铝沉淀.
解答 解:A.过量铁粉溶于稀HNO3中,反应生成硝酸亚铁、NO气体和水,正确的离子方程式为:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O,故A错误;
B.过量NaHSO4溶液加入到Ba(OH)2溶液中,反应生成硫酸钡沉淀、硫酸钠和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故B正确;
C.少量Cl2通人FeBr2溶液中,只有亚铁离子反应,正确的离子方程式为:2Fe2++Cl2═2 Cl-+2Fe2+,故C错误;
D.少量 AlCl3溶液滴入到氨水中,反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.下列结论错误的是( )
| A. | 氢化物的稳定性:HF>HCl>H2S>PH3>SiH4 | |
| B. | 微粒半径:K+>Al3+>S2->Cl- | |
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | |
| D. | 金属性:K>Ca>Mg>Be |
13.下列氧化还原反应的方程式配平正确的是( )
| A. | Fe3++S2-=Fe2++S | B. | Fe3++Fe=2Fe2+ | ||
| C. | Fe2++Cl2=Fe3++2Cl- | D. | 2Fe3++2I-=2Fe2++I2 |
7.满足分子式为C4H8ClBr的有机物共有( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
14.下列说法不正确的是( )
| A. | 利用丁达尔效应可区分蛋白质溶液与葡萄糖溶液 | |
| B. | 将饱和FeCl3溶液滴入沸水中,将继续煮沸至溶液呈红褐色即生成氢氧化铁胶体 | |
| C. | 用过滤法可以除去Fe(OH)3胶体中的FeCl3 | |
| D. | 用豆浆中加入硫酸钙制豆腐,是利用了胶体的聚沉性质 |
12.下列气体的制备和性质实验中,由现象得出的结论错误的是( )
| 选项 | 试剂 | 试纸/试液 | 现象 | 结论 |
| A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
| B | 浓盐酸、浓硫酸 | 紫色石蕊试纸 | 变红 | HCl为酸性气体 |
| C | 浓盐酸、二氧化锰 | 淀粉碘化钾试纸 | 变蓝 | Cl2具有氧化性 |
| D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
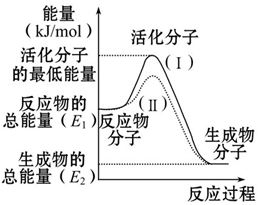 请认真观察如图,然后回答问题:
请认真观察如图,然后回答问题: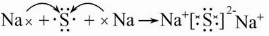 .
.